
Wetenschap
Wat is de evenwichtige chemische vergelijking voor stikstof en waterstof om ammoniak te vormen?
n₂ (g) + 3H₂ (g) → 2nh₃ (g)
Dit is wat de vergelijking betekent:
* n₂ (g): Stikstofgas (N₂) is een diatomisch molecuul in zijn gasvormige toestand.
* 3H₂ (g): Waterstofgas (H₂) is ook diatomeeën en in zijn gasvormige toestand.
* 2NH₃ (g): Ammoniak (NH₃) wordt geproduceerd in zijn gasvormige toestand.
Verklaring:
* het evenwicht tussen de vergelijking: De vergelijking is in evenwicht omdat er hetzelfde aantal atomen van elk element aan beide zijden van de vergelijking is.
* stikstof: 2 stikstofatomen aan beide zijden.
* waterstof: 6 waterstofatomen aan beide zijden.
* De reactie: Deze reactie is een voorbeeld van een combinatiereactie, waarbij twee of meer reactanten combineren om een enkel product te vormen. Het vereist een hoge temperatuur en de druk die zich voordoet.
Deze vergelijking is cruciaal om te begrijpen hoe ammoniak industrieel wordt gesynthetiseerd met behulp van het Haber-Bosch-proces.
 Warmte reist door geleiding wanneer de moleculen stoppen met beweegt rond waar of onwaar?
Warmte reist door geleiding wanneer de moleculen stoppen met beweegt rond waar of onwaar?  Is een zuur een stof die hydroxide-ionen produceert in een wateroplossing?
Is een zuur een stof die hydroxide-ionen produceert in een wateroplossing?  Hoe lassen werkt
Hoe lassen werkt  Nieuw koolstofnitride-materiaal in combinatie met ruthenium verbetert zichtbaar licht CO2-reductie in water
Nieuw koolstofnitride-materiaal in combinatie met ruthenium verbetert zichtbaar licht CO2-reductie in water Goedkoop, afdrukbaar 3D-apparaat ontworpen voor het analyseren van chemicaliën van smartphones
Goedkoop, afdrukbaar 3D-apparaat ontworpen voor het analyseren van chemicaliën van smartphones
 Hagedissen gevonden in Louisiana
Hagedissen gevonden in Louisiana Het is misschien mogelijk om de ijskappen opnieuw te bevriezen om de opwarming van de aarde te vertragen
Het is misschien mogelijk om de ijskappen opnieuw te bevriezen om de opwarming van de aarde te vertragen Niet-duurzame bodemerosie in delen van het VK
Niet-duurzame bodemerosie in delen van het VK Hoe verhoudt de wet van het behoud van behoud zich tot fotosynthese en ademhalingschemische vergelijkingen?
Hoe verhoudt de wet van het behoud van behoud zich tot fotosynthese en ademhalingschemische vergelijkingen?  Antarctische Circumpolaire Stroom stroomt sneller in warme fasen
Antarctische Circumpolaire Stroom stroomt sneller in warme fasen
Hoofdlijnen
- Als een lichaamscel 22 chromosomen heeft, wat zou de telling voor reproductieve cellen zijn?
- Wat zijn de planten die hun voedsel niet zelf kunnen bereiden?
- Nitrosomonas en nitrobacter zijn de twee belangrijkste geslachten van stikstofbevalling bacteriën waar of onwaar?
- Van Alaska tot Amazonia:de eerste wereldwijde kaarten met eigenschappen die de groei van vegetatie stimuleren
- Hoe een klein en vreemd zeedier gedurende zijn hele leven onbeperkt sperma produceert
- Onderzoek onthult opmerkelijke variabiliteit in de hittetolerantie van koraal
- Wat gebruiken cellen om stoffen te transporteren?
- Geen toverstaf nodig:wetenschappers stellen een manier voor om elke cel in een ander celtype te veranderen
- Waarom fruitvliegjes de eerste dieren in de ruimte waren
- Polymeren in meteorieten geven aanwijzingen voor het vroege zonnestelsel

- Een manier om kunstmatige intelligentie te gebruiken om chemische reacties te voorspellen
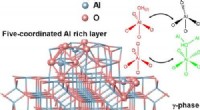
- Aard van vijf-gecoördineerd aluminium op γ-Al2O3-oppervlak
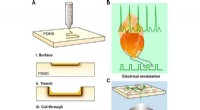
- Laserschrijven van met stikstof gedoteerd siliciumcarbide voor biologische modulatie
- Het licht zien:onderzoekers bieden oplossing voor efficiëntieprobleem van kunstmatige fotosynthese
 Hoeveel sneller wordt energie geproduceerd uit aerobe ademhaling?
Hoeveel sneller wordt energie geproduceerd uit aerobe ademhaling?  Wat is de energieoverdracht in een speelgoedauto?
Wat is de energieoverdracht in een speelgoedauto?  Wat hebben een brekende telescoop en reflecteren gemeen?
Wat hebben een brekende telescoop en reflecteren gemeen?  NASA's eerste vlucht naar de maan, Apollo8, markeert 50e verjaardag
NASA's eerste vlucht naar de maan, Apollo8, markeert 50e verjaardag Een aanpak voor het beveiligen van audioclassificatie tegen aanvallen van tegenstanders
Een aanpak voor het beveiligen van audioclassificatie tegen aanvallen van tegenstanders Welke golven hebben moleculen nodig om de energie over te dragen?
Welke golven hebben moleculen nodig om de energie over te dragen?  K2-25:Een excentrieke hete Neptunus met de massa van zeven aardes
K2-25:Een excentrieke hete Neptunus met de massa van zeven aardes Astronomen vinden een beroemde dubbelganger van exoplaneten
Astronomen vinden een beroemde dubbelganger van exoplaneten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

