
Wetenschap
Wat is de elektronenconfiguratie voor fluoratoom?
De elektronenconfiguratie voor een fluoratoom is:
1S² 2S² 2P⁵
Hier is hoe je het kunt begrijpen:
* 1S²: Het eerste energieniveau (n =1) heeft één sub -niveau, het 'S' Subblevel, dat maximaal 2 elektronen kan bevatten. Dus, fluor heeft 2 elektronen in zijn 1s orbitaal.
* 2S²: Het tweede energieniveau (n =2) heeft ook een 's subblevel, met nog eens 2 elektronen.
* 2p⁵: Het tweede energieniveau heeft een 'P' -subblevel, dat maximaal 6 elektronen kan bevatten. Fluor heeft 5 elektronen in zijn 2P -orbitalen.
Laat het me weten als je een meer gedetailleerde uitleg van elektronenconfiguraties wilt!
 Bossen hielden hun adem in tijdens de onderbreking van de opwarming van de aarde, uit onderzoek blijkt
Bossen hielden hun adem in tijdens de onderbreking van de opwarming van de aarde, uit onderzoek blijkt staat geoloog, partners maken nieuwe oppervlaktegeologische kaarten voor Massachusetts
staat geoloog, partners maken nieuwe oppervlaktegeologische kaarten voor Massachusetts Waterkwaliteit:een kwestie van perspectief
Waterkwaliteit:een kwestie van perspectief Wat zijn de drie druk die leiden tot biodiversiteit volgens de theorie van eilandbiogeografie?
Wat zijn de drie druk die leiden tot biodiversiteit volgens de theorie van eilandbiogeografie?  Vervuiling door fossiele brandstoffen veroorzaakt wereldwijd een op de vijf sterfgevallen:studie
Vervuiling door fossiele brandstoffen veroorzaakt wereldwijd een op de vijf sterfgevallen:studie
Hoofdlijnen
- Waarom zijn cellen belangrijk voor levende organismen?
- Namen van DNA-strengen
- Wat is Supplex Nylon?
- De sociale wetenschappen die zich bezighoudt met het gedrag en het denken aan organismen?
- Ideeën voor celademhaling
- Glycosylering - onbekend terrein in kaart brengen
- Hoeveel zintuigen heeft een mens?
- Geef de biologische betekenis van celademhaling?
- Wat geloven mensen over de flogistontheorie?
- Nieuw inzicht in de oppervlakte-eigenschappen van tweedimensionale MXenes-materialen

- Hier is een draai aan een eeuwenoude klassieker:Lactosevrije chocolademelk

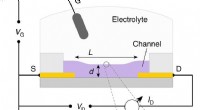
- Nieuwe methode benchmarkt organische gemengde geleiders
- Nieuwe biomaterialen kunnen worden verfijnd voor medische toepassingen

- Een eenvoudige methode ontwikkeld voor 3D-biofabricage op basis van bacteriële cellulose

 Quantum dot witte LED's bereiken een recordrendement
Quantum dot witte LED's bereiken een recordrendement Hoe wordt erts uit de grond gehaald?
Hoe wordt erts uit de grond gehaald?  Hoe gebeurt meteorietbotsing?
Hoe gebeurt meteorietbotsing?  Atomair gedispergeerd Ni is cokesbestendig voor droge reforming van methaan
Atomair gedispergeerd Ni is cokesbestendig voor droge reforming van methaan Als de absolute temperatuur van een radiator wordt verdubbeld door welke factor verandert stralend vermogen?
Als de absolute temperatuur van een radiator wordt verdubbeld door welke factor verandert stralend vermogen?  Welk type energie is geassocieerd met willekeurig bewegende deeltjes in een monstergas?
Welk type energie is geassocieerd met willekeurig bewegende deeltjes in een monstergas?  Wetenschappers bepalen precieze 3D-locatie, identiteit van alle 23, 000 atomen in een nanodeeltje
Wetenschappers bepalen precieze 3D-locatie, identiteit van alle 23, 000 atomen in een nanodeeltje Is de aarde een elektrisch geladen object?
Is de aarde een elektrisch geladen object?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

