
Wetenschap
Wat is de netto ionische vergelijking voor de reactie van aluminiumhydroxide met een overtollige geconcentreerde natriumoplossing?
1. Schrijf de gebalanceerde moleculaire vergelijking:
AL (OH) ₃ (S) + 3NAOH (AQ) → Na₃al (OH) ₆ (aq)
2. Schrijf de volledige ionische vergelijking:
AL (OH) ₃ (S) + 3NA⁺ (AQ) + 3OH⁻ (AQ) → 3NA⁺ (AQ) + [AL (OH) ₆] ³⁻ (aq)
3. Identificeer en annuleer toeschouwersionen:
Toeschouwersionen zijn die die aan beide zijden van de vergelijking ongewijzigd verschijnen. In dit geval is het toeschouwer -ion na⁺.
4. Schrijf de netto ionische vergelijking:
AL (OH) ₃ (S) + 3OH⁻ (AQ) → [AL (OH) ₆] ³⁻ (aq)
Verklaring:
* aluminium hydroxide (AL (OH) ₃) is een vaste stof, dus het breekt niet uit elkaar in ionen.
* Natriumhydroxide (NaOH) is een sterke basis die volledig dissocieert in oplossing, waardoor Na⁺ en OH⁻ -ionen worden gevormd.
* Natriumaluminaat (Na₃al (OH) ₆) is een complexe ion die in oplossing bestaat.
De netto ionische vergelijking toont aan dat aluminiumhydroxide reageert met hydroxide -ionen om het tetrahydroxoaluminaat (iii) complexion te vormen, [AL (OH) ₆] ³⁻.
Sleutelpunten:
* Overtollige NaOH: De reactie vereist overtollige NaOH om de vorming van de complex ion te stimuleren.
* Amfoterische aard: Aluminiumhydroxide is amfoterisch, wat betekent dat het kan reageren met zowel zuren als basen. In dit geval fungeert het als een zuur en accepteert het hydroxide -ionen.
* Complex ionenvorming: De reactie vormt een complexe ion, een soort die een centraal metaalion bevat omringd door liganden (in dit geval hydroxide -ionen).
 Wat is het oxidatiegetal van elk atoom in S2Cl2?
Wat is het oxidatiegetal van elk atoom in S2Cl2?  Is koolstofdisulfide polair of niet-polair?
Is koolstofdisulfide polair of niet-polair?  Welke klasse elementen worden naast waterstof en zuurstof in zuren gevonden?
Welke klasse elementen worden naast waterstof en zuurstof in zuren gevonden?  Onderzoekers maken de volgende generatie, batterijcomponent met hoge taaiheid
Onderzoekers maken de volgende generatie, batterijcomponent met hoge taaiheid Waarom zijn de kalium- en nitraationen niet betrokken bij de evenwichtsreactie?
Waarom zijn de kalium- en nitraationen niet betrokken bij de evenwichtsreactie?
 NASA-NOAA-satelliet toont omvang van Irmas-restanten
NASA-NOAA-satelliet toont omvang van Irmas-restanten Onderzoek toont aan dat regio's steeds vaker last hebben van warme, droge omstandigheden tegelijkertijd
Onderzoek toont aan dat regio's steeds vaker last hebben van warme, droge omstandigheden tegelijkertijd Waarom verschijnen groene planten voor ons?
Waarom verschijnen groene planten voor ons?  Gezondere lucht door de lage-emissiezone
Gezondere lucht door de lage-emissiezone Meststoffen passen de stikstofcyclus van prairieplanten aan, volgens nieuwe studie
Meststoffen passen de stikstofcyclus van prairieplanten aan, volgens nieuwe studie
Hoofdlijnen
- Een model waarmee planten hun fotosynthetische stofwisseling aanpassen aan de lichtintensiteit
- Onderzoekers ontdekken wat pneumokokken je ziek maken
- Wat is de term die het tegenovergestelde van dorsaal betekent?
- Hoe bacteriën zwemmen:onderzoekers ontdekken nieuwe mechanismen
- Wat is het proces van blaasjes die hun inhoud buiten de cel vrijgeven?
- Wat is het effect van natrium op de kieming van planten?
- Baanbrekende veldproeven tonen het potentieel van genbewerking in gewassen aan
- Wat is het ontginnen van hypothesen?
- Mitotische celdeling is geïnitieerd in de?
- Onderzoekers onderzoeken het gebruik van nieuwe materialen om efficiëntere zonnecellen te maken

- Vogels op grote hoogte ontwikkelen vergelijkbare eigenschappen via verschillende mutaties

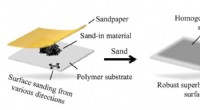
- Water kan dit geschuurde, gepoederde oppervlak niet raken
- Nieuwe biologische en veiligere zepen

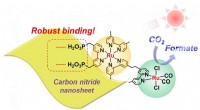
- Nieuw koolstofnitride-materiaal in combinatie met ruthenium verbetert zichtbaar licht CO2-reductie in water
 Eiwit beëindigt opzettelijk de eigen synthese door de synthesemachinerie te destabiliseren - het ribosoom
Eiwit beëindigt opzettelijk de eigen synthese door de synthesemachinerie te destabiliseren - het ribosoom Wat is een reiziger de sterren van Space Shuttle gezien?
Wat is een reiziger de sterren van Space Shuttle gezien?  Meer dan een lenteschoonmaak voor LHC-magneten
Meer dan een lenteschoonmaak voor LHC-magneten 3D-weergave van Amazonebossen legt de effecten van El Nino-droogte vast
3D-weergave van Amazonebossen legt de effecten van El Nino-droogte vast Coherente oscillatie tussen fononen en magnons
Coherente oscillatie tussen fononen en magnons Materiaalchemici tappen lichaamswarmte af om slimme kleding van stroom te voorzien
Materiaalchemici tappen lichaamswarmte af om slimme kleding van stroom te voorzien Nieuwe eigenschappen van kosmische straling, silicium, magnesium en neon gevonden door Alpha Magnetic Spectrometer aan boord van ISS
Nieuwe eigenschappen van kosmische straling, silicium, magnesium en neon gevonden door Alpha Magnetic Spectrometer aan boord van ISS Wat is het Higgs-deeltje precies?
Wat is het Higgs-deeltje precies?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

