
Wetenschap
Wat heeft het hogere smeltpunt natriumchloride of aluminiumoxide?
* ionische bindingssterkte: Beide verbindingen zijn ionisch, wat betekent dat ze bij elkaar worden gehouden door elektrostatische attracties tussen positief geladen ionen (kationen) en negatief geladen ionen (anionen).
* aluminiumoxide: Aluminium heeft een +3 lading en zuurstof heeft een -2 lading, wat leidt tot een sterke elektrostatische aantrekkingskracht.
* Natriumchloride: Natrium heeft een +1 lading en chloor heeft een -1 lading, wat resulteert in een zwakkere elektrostatische aantrekkingskracht in vergelijking met aluminiumoxide.
* roosterstructuur: De opstelling van ionen in een kristalrooster speelt ook een rol. Aluminiumoxide heeft een strengste en stabiele kristalstructuur dan natriumchloride, waardoor het moeilijker is om uit elkaar te breken.
smeltpunten:
* aluminiumoxide (al₂o₃): ~ 2072 ° C (3761 ° F)
* Natriumchloride (NaCl): ~ 801 ° C (1474 ° F)
Het aanzienlijk hogere smeltpunt van aluminiumoxide is een direct gevolg van zijn sterkere ionische bindingen en stabielere kristalstructuur.
Hoofdlijnen
- Eén molecuul glucose maakt hoeveel moleculen ATP?
- Kunstmatig leven
- Waarom zijn sommige E. coli dodelijk terwijl andere vreedzaam in ons lichaam leven?
- Chemotaxonomie en het belang ervan bij de classificatie van planten?
- Wat is een maat voor de organismen van het aantal variëteiten en de amp -variabiliteit in een ecosysteem?
- Hoe muizen de beste ontsnappingsroute kiezen
- Vreemde zijde:waarom abseilende spinnen niet uit de hand lopen
- Nectarivoren:een wereld van zoetekauwen
- Hoe schakelen gewas-veeteeltsystemen over naar groene landbouwontwikkeling in het Baiyangdian Basin?
- Elektronische vaste stof kan de CO2-uitstoot in koelkasten en airconditioners verminderen

- Nieuwe milieuvriendelijke vleesanaloog gezonder, biedt meer smaken

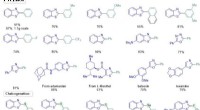
- Kruiskoppelingsreacties:semiheterogene op PCN-Cu gebaseerde metallafotokatalyse
- Wetenschappers zorgen voor doorbraak vitamine B12

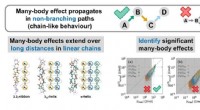
- Wanneer zijn veellichaamseffecten significant?
 Is een astronomische eenheid groter dan een lichtjaar?
Is een astronomische eenheid groter dan een lichtjaar?  Het einde van nepnieuws
Het einde van nepnieuws Wat zijn de overeenkomsten in het moderne periodiek systeem en de tabel?
Wat zijn de overeenkomsten in het moderne periodiek systeem en de tabel?  Tevredenheid politie in ontwikkelingslanden afhankelijk van minder corruptie
Tevredenheid politie in ontwikkelingslanden afhankelijk van minder corruptie Onderzoekers ontwikkelen een systeem om te beoordelen hoe effectief soorten zijn bij het bestuiven van gewassen
Onderzoekers ontwikkelen een systeem om te beoordelen hoe effectief soorten zijn bij het bestuiven van gewassen  Wat betekent de rechtszaak van Epic Games v. Apple voor iPhone-bezitters?
Wat betekent de rechtszaak van Epic Games v. Apple voor iPhone-bezitters? Wat zijn de lagen van een berg?
Wat zijn de lagen van een berg?  Wanneer moet iemand de voorspellingen van een AI-assistent vertrouwen?
Wanneer moet iemand de voorspellingen van een AI-assistent vertrouwen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


