
Wetenschap
Wat is de hydroxide -ionenconcentratie in een waterige oplossing die hydronium 0,13 m?
Inzicht in de relatie
* kw (ionenproductconstante van water): Het product van de hydroniumionconcentratie ([H3O+]) en de hydroxide-ionenconcentratie ([OH-]) in water is altijd een constante bij een gegeven temperatuur. Deze constante wordt KW genoemd en heeft een waarde van 1,0 x 10^-14 bij 25 ° C.
* Vergelijking: KW =[H3O+] [OH-]
Berekening
1. Begin met de gegeven hydroniumionconcentratie: [H3O+] =0,13 m
2. Gebruik de KW -vergelijking om op te lossen voor de hydroxide -ionenconcentratie:
* 1,0 x 10^-14 =(0,13 m) * [oh-]
* [Oh-] =(1,0 x 10^-14) / (0,13 m)
* [Oh-] ≈ 7,7 x 10^-14 m
Antwoord: De hydroxide-ionenconcentratie in de oplossing is ongeveer 7,7 x 10^-14 M.
 Wat is de algemene pH van witte thee?
Wat is de algemene pH van witte thee?  Wat zijn de producten van neutralisatiereactie tussen NHO3 en CA (OH) 2?
Wat zijn de producten van neutralisatiereactie tussen NHO3 en CA (OH) 2?  Wat is de juiste verbinding voor CR2O3?
Wat is de juiste verbinding voor CR2O3?  Een eenstaps multikatalytische methode om racemische mengsels te verrijken tot een enkele enantiomeer
Een eenstaps multikatalytische methode om racemische mengsels te verrijken tot een enkele enantiomeer Wat is de speciale naam voor chemische reactie tussen een zuur en een alkali?
Wat is de speciale naam voor chemische reactie tussen een zuur en een alkali?
 Welke wetenschapstak heeft 4 fundamentele principes?
Welke wetenschapstak heeft 4 fundamentele principes?  Nieuw klimaatmodel voor het IPCC
Nieuw klimaatmodel voor het IPCC Palmolie decimerende dieren in het wild, oplossingen ongrijpbaar:rapport
Palmolie decimerende dieren in het wild, oplossingen ongrijpbaar:rapport Weersatelliet dwaalt door de tijd, ruimte, verdwaalde opwarming veroorzaken om gegevens te besmetten
Weersatelliet dwaalt door de tijd, ruimte, verdwaalde opwarming veroorzaken om gegevens te besmetten Wat was het tweede organisme dat op aarde verscheen?
Wat was het tweede organisme dat op aarde verscheen?
Hoofdlijnen
- Waarom is UV-licht schadelijk?
- Welke vlinderbloemige boom produceert senna?
- Hoe zijn cellulaire ademhaling in cellen en verbranding?
- Wetenschappers visualiseren hoe bacteriën met elkaar praten
- Welke bacteriën eten de leukocyten?
- Hoe verwerf je aangeboren gedrag?
- Wat is een TE -microscoop?
- Moleculen A en B komen in contact met het celmembraan van hetzelfde molecuul passeert gemakkelijk, maar molecuul konden niet welke verklaring moleculen een?
- Welke verklaring verklaart Mendels -observaties over hoe eigenschappen van generatie op generatie worden doorgegeven?
- Chemici maken circulaire fluorescerende kleurstoffen voor biologische beeldvorming
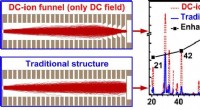
- Verbetering van de efficiëntie van de ionentransmissie van massaspectrometers
- Op zoek naar wanorde als katalysator voor verandering

- Stijve, pijnlijke knieën? In het laboratorium gemaakte kraakbeengel presteert beter dan het echte werk

- Ingenieurs maken microfluïdica modulair met behulp van de populaire in elkaar grijpende blokken

 Honderden geëvacueerd nadat angstaanjagende overstromingen Nieuw-Zeeland troffen
Honderden geëvacueerd nadat angstaanjagende overstromingen Nieuw-Zeeland troffen Nanodeeltjes vormen onder druk superkristallen
Nanodeeltjes vormen onder druk superkristallen Heldere gebieden op Ceres suggereren geologische activiteit
Heldere gebieden op Ceres suggereren geologische activiteit Onderzoekers ontwikkelen plantaardige technologie die biobrandstoffen helpt, kan kanker bestrijden
Onderzoekers ontwikkelen plantaardige technologie die biobrandstoffen helpt, kan kanker bestrijden Opvallende nieuwe opname van het statige sterrenstelsel Messier 106, gemaakt met de Nicholas U. Mayall 4-meter Telescope
Opvallende nieuwe opname van het statige sterrenstelsel Messier 106, gemaakt met de Nicholas U. Mayall 4-meter Telescope Hoe lang is de zonsondergang, vanaf moment dat de zon horizon raakt totdat deze volledig verdwijnt?
Hoe lang is de zonsondergang, vanaf moment dat de zon horizon raakt totdat deze volledig verdwijnt?  Waarom is de valentie van natrium?
Waarom is de valentie van natrium?  Zigzaggend apparaat focust hoogenergetische stralingsemissies
Zigzaggend apparaat focust hoogenergetische stralingsemissies
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

