
Wetenschap
Volgens de Gibbs Free Energy -vergelijking Wat is het temperatuurbereik voor welke vorming van vloeibare broom spontaan?
Inzicht in de concepten
* Gibbs Free Energy (ΔG): Een thermodynamische hoeveelheid die de spontaniteit van een proces voorspelt.
* spontaan proces (ΔG <0): Een proces dat optreedt zonder externe invoer van energie.
* Enthalpy (ΔH): De warmte die tijdens een proces is geabsorbeerd of vrijgegeven.
* entropie (δs): Een maat voor de aandoening of willekeur van een systeem.
* Gibbs Free Energy -vergelijking: Δg =ΔH - Tδs
De concepten toepassen op Bromine
1. Identificeer het proces: We zijn geïnteresseerd in de vorming van vloeibare broom (Br₂) uit de gasvormige toestand. Dit kan worden weergegeven als:
Br₂ (G) → Br₂ (L)
2. Bepaal enthalpie en entropiewijzigingen:
* ΔH (enthalpy -verandering): Het proces van het vormen van vloeibare broom uit gas is exotherm, wat betekent dat warmte wordt vrijgegeven. Dus, AH is negatief.
* ΔS (entropie -verandering): Vloeistoffen zijn meer geordend dan gassen. Daarom is de entropieverandering negatief (ΔS <0) omdat het systeem meer wordt geordend.
3. Spontane vorming: Om de vorming van vloeibare broom spontaan te laten zijn, moet ΔG negatief zijn.
* ΔG <0: Omdat AH negatief is en AS negatief is, is de enige manier om ervoor te zorgen dat AG negatief is, als de term `-Tδs` groot genoeg is om op te wekken tegen de negatieve AH. Dit betekent dat de temperatuur (t) hoog genoeg moet zijn.
Conclusie
Er is een specifiek temperatuurbereik waar de vorming van vloeibare broom spontaan is:
* Bij lage temperaturen: De `-TAS'-term is klein en de negatieve A domineert, waardoor Ag negatief wordt. Dit bevordert de vorming van vloeibare broom.
* bij hoge temperaturen: De `-TAS'-term wordt groter, waardoor Ag positief wordt. Dit bevordert de vorming van gasvormige broom.
belangrijke opmerkingen:
* Het exacte temperatuurbereik hangt af van de specifieke waarden van AH en AS voor het proces. U moet deze waarden opzoeken of experimenten uitvoeren om ze te bepalen.
* De faseovergang tussen vloeistof en gasvormige broom wordt ook beïnvloed door druk.
Laat het me weten als je wilt dat ik een van deze punten uitwerk!
 De efficiëntie van systemen voor het opvangen en omzetten van koolstof verhogen
De efficiëntie van systemen voor het opvangen en omzetten van koolstof verhogen Natuurkundigen maken een model om de eigenschappen van elk molecuul te voorspellen
Natuurkundigen maken een model om de eigenschappen van elk molecuul te voorspellen Doorbraak metaalionen leidt tot nieuwe biomaterialen
Doorbraak metaalionen leidt tot nieuwe biomaterialen In een bol wordt edelgas argon gebruikt. waarom in plaats van lucht in de gloeilamp?
In een bol wordt edelgas argon gebruikt. waarom in plaats van lucht in de gloeilamp?  Waarom is koolstofdioxide geen organische verbinding?
Waarom is koolstofdioxide geen organische verbinding?
 Onderzoek identificeert vingerafdrukken van klimaatverandering en aansprakelijkheid van emittenten
Onderzoek identificeert vingerafdrukken van klimaatverandering en aansprakelijkheid van emittenten Instructies voor een Egg Drop Science Fair Project
Instructies voor een Egg Drop Science Fair Project Bladverliezende Bos Biome Feiten voor Kids
Bladverliezende Bos Biome Feiten voor Kids Waren in het tijdperk van overtoerisme, maar er is een duurzamere weg vooruit
Waren in het tijdperk van overtoerisme, maar er is een duurzamere weg vooruit Duurzaam zuivelproject vindt manieren om emissies te verlagen, winst verhogen
Duurzaam zuivelproject vindt manieren om emissies te verlagen, winst verhogen
Hoofdlijnen
- Wat is de stikstofgroep?
- Wat is de beste beschrijving van evolutie camouflage door natuurlijke selectie?
- Wordt cytoplasma tot zowel planten- als diercellen behoord?
- Wat is wetenschappelijk tijdschrift?
- Profase: wat gebeurt er in dit stadium van mitose en meiose?
- Wat zijn toepassingen van mitose en meoisis?
- Uit onderzoek blijkt dat het verlies van grote herbivoren de interacties tussen planten en hun natuurlijke vijanden beïnvloedt
- Waarom malariaparasieten sneller zijn dan menselijke immuuncellen
- Superbug-onderzoek onthult hoe de E. coli-stam dodelijke krachten verwierf
- Nieuwe techniek voor het bestuderen van roesten van staal komt de mijnbouwsector ten goede

- Metalen nanokatalysatoren imiteren de structuur van enzymen

- Nieuwe methode keert de zelfassemblage van vloeibare kristallen om

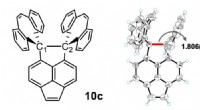
- Nieuw record voor lengte koolstof-koolstof enkelvoudige binding
- Durian skin-biocomposiet voor afhaalcontainers en 3D-printen

 Hoe vergroten mensen verwering en erosie?
Hoe vergroten mensen verwering en erosie?  Maximale steun voor migrantenjongeren in de hele EU
Maximale steun voor migrantenjongeren in de hele EU Kunnen astronomen radar gebruiken om een cataclysmische asteroïde te ontdekken?
Kunnen astronomen radar gebruiken om een cataclysmische asteroïde te ontdekken?  Welk type energie wordt geassocieerd met het willekeurige bewegingsdeeltje in een monstergas?
Welk type energie wordt geassocieerd met het willekeurige bewegingsdeeltje in een monstergas?  Onderzoekers onderzoeken hersenziekte-veroorzakende eiwitten op atomair niveau
Onderzoekers onderzoeken hersenziekte-veroorzakende eiwitten op atomair niveau Het proces waarmee atomaire kernen samen worden gecombineerd om een nieuw element te vormen, wordt aangeroepen.?
Het proces waarmee atomaire kernen samen worden gecombineerd om een nieuw element te vormen, wordt aangeroepen.?  Verbergen of opgegeten worden, urinechemicaliën vertellen modderkrabben
Verbergen of opgegeten worden, urinechemicaliën vertellen modderkrabben NASA deelt lijst met kosmische doelen voor eerste beelden van Webb-telescopen
NASA deelt lijst met kosmische doelen voor eerste beelden van Webb-telescopen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

