
Wetenschap
Een stuk ijzer met een gewicht van 85,65 g werd in lucht verbrand de massa De geproduceerde oxide 118,37 Molair gebruiken om gebruikte mollen om te zetten?
1. Bepaal de massa zuurstof
* De zuurstofmassa die met het ijzer reageerde, is het verschil tussen de massa van het oxide en de massa van het ijzer:
* Massa van zuurstof =118,37 g - 85,65 g =32,72 g
2. Converteren massa's naar mollen
* ijzer (Fe):
* Molaire massa Fe =55.845 g/mol
* Mol Fe =(85,65 g) / (55,845 g / mol) =1.534 mol
* zuurstof (O):
* Molaire massa van o =16,00 g/mol
* Mol o =(32,72 g) / (16,00 g / mol) =2,045 mol
3. Bepaal de empirische formule
* Verdeel het aantal mol mol van elk element door het kleinste aantal mol om de eenvoudigste verhouding van het hele nummer te krijgen:
* Fe:1.534 mol / 1.534 mol =1
* O:2.045 mol / 1.534 mol =1,33
* Aangezien we hele getallen nodig hebben, vermenigvuldig beide verhoudingen met 3 om te krijgen:
* Fe:3
* O:4
4. De empirische formule
* De empirische formule van het ijzeroxide is fe₃o₄ .
Opmerking: Dit is de formule voor een specifiek ijzeroxide genaamd magnetiet.
 Lab-on-a-chip-test heeft potentieel om COVID-19-immuunrespons sneller te detecteren dan huidige antilichaamtesten
Lab-on-a-chip-test heeft potentieel om COVID-19-immuunrespons sneller te detecteren dan huidige antilichaamtesten De formule voor zwavelzuur is H2SO4. Hoeveel mol zou een mol hebben?
De formule voor zwavelzuur is H2SO4. Hoeveel mol zou een mol hebben?  Onderzoek naar schone lucht zet giftige luchtverontreinigende stoffen om in industriële chemicaliën
Onderzoek naar schone lucht zet giftige luchtverontreinigende stoffen om in industriële chemicaliën Wat zijn de cijfers voor elk element of molecuul?
Wat zijn de cijfers voor elk element of molecuul?  Welk materiaal vormt as en puim?
Welk materiaal vormt as en puim?
 Nieuw onderzoek laat zien hoe de opwarming van de aarde onze regenval in de war brengt
Nieuw onderzoek laat zien hoe de opwarming van de aarde onze regenval in de war brengt  Amerikaanse energieachterblijvers voldoen nog steeds niet aan Parijs:analyse
Amerikaanse energieachterblijvers voldoen nog steeds niet aan Parijs:analyse Insecten vangen op kleur:zal het werken in Montana?
Insecten vangen op kleur:zal het werken in Montana?  Kleine satellieten onthullen de waterdynamiek in duizenden noordelijke meren
Kleine satellieten onthullen de waterdynamiek in duizenden noordelijke meren Het ontdekken van de geheimen van de betekenis en genezende eigenschappen van Tigers Eye
Het ontdekken van de geheimen van de betekenis en genezende eigenschappen van Tigers Eye
Hoofdlijnen
- Proteomische analyse laat zien hoe fosfiet bijdraagt aan de strijd tegen chemisch resistente afsterving
- Een kenmerk van het spijsverteringsepitheel dat het expansieorgaan ondersteunt, is de aanwezigheid van?
- De virale reproductieve cyclus waarin een faag zijn DNA in gastheercel injecteert en de metabole machines gebruikt om nieuwe fagen te produceren, veroorzaakt dan dat breuk wordt genoemd welke cyclus?
- Wetenschappers vinden bloedmolecuul dat wolven aantrekt stoot mensen af
- Wat zijn de sporten op het DNA Dubbelschroef gemaakt van?
- Welke structurele rol spelen fosfolipiden in cellen?
- Waarom is er geen nucleus in RBC en geplandters?
- Immuunfunctie geremodelleerd door mitochondriale vorm
- Het team vindt direct bewijs van rondtrekkende broedvogelsoorten aan de oostkust
- Gezondheidsbehandeling door chemische synthese

- Waterzuiveringssysteem gemaakt van hout, met hulp van een magnetron

- Onderzoekers demonstreren een fundamenteel nieuwe benadering van echografie

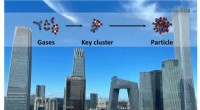
- Verborgen zuur-base clusters zorgen voor snelle vorming van atmosferische ultrafijne deeltjes
- Kookchemie minus hitte is gelijk aan nieuwe niet-giftige lijm

 Hoeveel zon heeft het plant -apengras nodig?
Hoeveel zon heeft het plant -apengras nodig?  Bepalen welke samenstelling meer is Acidic
Bepalen welke samenstelling meer is Acidic Chemicaliën gebruikt in warmtepakketten
Chemicaliën gebruikt in warmtepakketten  Elektronen aan de rand:atomair dunne materialen voor kwantumspinhallen
Elektronen aan de rand:atomair dunne materialen voor kwantumspinhallen Wat is minder nauwkeurig aan een Mercator -projectie?
Wat is minder nauwkeurig aan een Mercator -projectie?  Hoe celprocessen beschadigde eiwitten verzamelen en dumpen
Hoe celprocessen beschadigde eiwitten verzamelen en dumpen  Wat veroorzaakte de westelijke expansie van de Verenigde Staten?
Wat veroorzaakte de westelijke expansie van de Verenigde Staten?  Waarom wordt Radon nog steeds in de natuur gevonden?
Waarom wordt Radon nog steeds in de natuur gevonden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

