
Wetenschap
Waarom produceert een fles chloride silicium stomende dampen wanneer opengelaten op de bank maar koolstof niet?
Dit is waarom:
* siliciumchloride (SICL4) is zeer reactief met water: Bij blootstelling aan lucht reageert SICL4 krachtig met waterdamp aanwezig in de atmosfeer. Deze reactie produceert zoutzuur (HCL) en siliciumdioxide (SiO2), die zowel zeer corrosief als vluchtig zijn. Het HCL -gas is verantwoordelijk voor de stomende dampen die u waarneemt.
* De reactie:
SICL4 (L) + 2 H2O (G) → SiO2 (S) + 4 HCl (G)
* Koolstof is relatief inert: Koolstof is veel minder reactief dan siliciumchloride. Het reageert niet gemakkelijk met water of vocht in de lucht. Daarom produceert het geen zichtbare dampen.
Samenvattend: Siliciumchloride is zeer reactief met vocht en produceert zoutzuurgas, waardoor de stomende dampen worden veroorzaakt. Koolstof daarentegen is relatief inert en reageert niet met vocht, wat resulteert in geen zichtbare dampen.
 Video:Brengen menselijke begrafenispraktijken de ecosystemen van de aarde in de war?
Video:Brengen menselijke begrafenispraktijken de ecosystemen van de aarde in de war? Milieuvriendelijke rode verblindingsraket verandert vuurwerk, soldaat technologie
Milieuvriendelijke rode verblindingsraket verandert vuurwerk, soldaat technologie Hoe de zuiverheid van een zoutverbinding te bepalen
Hoe de zuiverheid van een zoutverbinding te bepalen  Welke metalen verbinden zich met andere elementen met behulp van metalen binding?
Welke metalen verbinden zich met andere elementen met behulp van metalen binding?  Hoeveel atomen zijn er in de 3e schaal een atoom met 4 schelpen?
Hoeveel atomen zijn er in de 3e schaal een atoom met 4 schelpen?
 Beleid dat is ontworpen om de volksgezondheid tegen fracking te beschermen, kan in de praktijk ondoeltreffend zijn
Beleid dat is ontworpen om de volksgezondheid tegen fracking te beschermen, kan in de praktijk ondoeltreffend zijn Hoe planten de poriën waardoor ze ademen spreiden
Hoe planten de poriën waardoor ze ademen spreiden  Zelfs zonder het schone energieplan, VS kunnen emissiereducties in de Overeenkomst van Parijs bereiken
Zelfs zonder het schone energieplan, VS kunnen emissiereducties in de Overeenkomst van Parijs bereiken Planten die in grotten wonen
Planten die in grotten wonen De drijvende kracht achter tropische modderstromen
De drijvende kracht achter tropische modderstromen
Hoofdlijnen
- Moeten we de genen van buitengewone mensen sparen voor klonen?
- Hoe blijven de bacteriën niet -besmet wanneer het enigszins ajar bedekt na het gieten van voedingsagar in petrischalen?
- Zijn weg naar de top vinden:hoe een celoppervlakreceptor zijn bestemming bereikt
- Bidsprinkhanengarnalen hebben de beste ogen ter wereld, maar waarom?
- Wat zijn de delen belangrijker in het menselijk lichaam?
- Welke delen van de cel zijn in theorie opgenomen?
- Hoe vissen tegelijkertijd geluiden horen en maken
- Welke techniek zou een wetenschapper gebruiken om specifieke organel te isoleren?
- Wat zijn de belangrijkste functies van eenvoudige koolhydraten in levende wezens?
- Wederopstanding van quasikristallen:bevindingen maken een exotisch materiaal commercieel levensvatbaar

- Nieuwe microscooptechniek onthult interne structuur van levende embryo's
- Doorbraak in ionenwindtechnologie neemt een vlucht

- Goedkope hernieuwbare energie:het fotosyntheseproces doorbreken dat planten in staat stelt om wat te splitsen

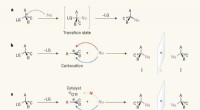
- Een SN1-reactie gebruiken om quaternaire stereocentra te maken
 Wetenschappers registreren sterke toroïdale dipoolrespons in breed frequentiebereik
Wetenschappers registreren sterke toroïdale dipoolrespons in breed frequentiebereik Welk element deelt de meeste kenmerken met magnesium (mg)?
Welk element deelt de meeste kenmerken met magnesium (mg)?  Na de crisis:hoe we (een deel van) onze misleidende overtuigingen kunnen vermijden
Na de crisis:hoe we (een deel van) onze misleidende overtuigingen kunnen vermijden  'S Werelds grootste batterij in Australië om Musks te overtroeven
'S Werelds grootste batterij in Australië om Musks te overtroeven Hoeveel water maakt 1 kopje ijs?
Hoeveel water maakt 1 kopje ijs?  Grote hiaten in onderzoek naar microplastics in Noord-Amerika, studie vondsten
Grote hiaten in onderzoek naar microplastics in Noord-Amerika, studie vondsten Wat is een sculptuur die opkomt van een plat oppervlak?
Wat is een sculptuur die opkomt van een plat oppervlak?  Wat doet water met een rots?
Wat doet water met een rots?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

