
Wetenschap
Geef de moleculaire formule van verbinding die empirische CHCL heeft met een kolf van 256 ml bij 373 K en 750 Torr bevat 0,800 G gasvormige verbinding?
1. Bereken de mol van de verbinding:
* Gebruik de ideale gaswet:PV =NRT
* P =druk =750 torr =750/760 atm
* V =volume =256 ml =0,256 l
* n =aantal mol (wat we willen vinden)
* R =ideale gasconstante =0,0821 l · atm/mol · k
* T =temperatuur =373 K
* Herschik de vergelijking om op te lossen voor n:
n =(pv)/(rt)
n =(750/760 atm * 0,256 l)/(0.0821 l · atm/mol · k * 373 k)
n ≈ 0,0082 mol
2. Bereken de molaire massa van de verbinding:
* Molaire massa =massa / mol
* Molaire massa =0,800 g / 0,0082 mol
* Molaire massa ≈ 97,56 g/mol
3. Bepaal de empirische formulemassa:
* Empirische formule:Chcl
* Empirische formulemassa:12.01 g/mol (c) + 1,01 g/mol (H) + 35,45 g/mol (CL) =48,47 g/mol
4. Zoek de verhouding van de molaire massa tot de empirische formulemassa:
* Verhouding =molaire massa / empirische formulemassa
* Verhouding =97,56 g/mol/48,47 g/mol ≈ 2
5. Bepaal de moleculaire formule:
* Omdat de verhouding ongeveer 2 is, is de moleculaire formule tweemaal de empirische formule:
* Moleculaire formule =(chcl) ₂ = c₂h₂cl₂
Daarom is de moleculaire formule van de verbinding c₂h₂cl₂.
 Noorse vurenziekten en -behandelingen
Noorse vurenziekten en -behandelingen Bio vliegtuigbrandstoffen goed voor het klimaat, maar technologieën moeten worden aangepast
Bio vliegtuigbrandstoffen goed voor het klimaat, maar technologieën moeten worden aangepast Het verminderen van het broeikasgas in de Rocky Mountain-regio is gezond, financiele voordelen
Het verminderen van het broeikasgas in de Rocky Mountain-regio is gezond, financiele voordelen Ongewone sneeuw doodt 4, brengt een groot deel van Spanje tot stilstand
Ongewone sneeuw doodt 4, brengt een groot deel van Spanje tot stilstand Waar groeit de mos?
Waar groeit de mos?
Hoofdlijnen
- Is CLITOCYBE dealbata een symbiont saprofyt of parasiet?
- Hoe bepalen chromosomen seks?
- Wat als we een einde maken aan de hongersnood?
- Een biosyntheseroute kan worden gekarakteriseerd als?
- Klimaatverandering maakt baardagamen mogelijk minder intelligent
- Hommels kunnen volgens de Californische instandhoudingswet als vissen worden geclassificeerd, zegt de rechtbank
- Wie is dominanter de mannelijke of vrouwelijke moordende walvis?
- De vogelgriep veroorzaakt duizenden zeehondensterfte. Wetenschappers weten niet zeker hoe ze dit kunnen vertragen
- Onderzoekers tonen aan dat RNA-ribozymen in staat zijn om samen te werken en zichzelf weer in elkaar te zetten
- Recycling van plastic:vinylpolymeer afgebroken tot aspirinecomponenten

- De milieukosten van contactlenzen

- Unboil een eiermachine zorgt voor een verbeterde bacteriedetector
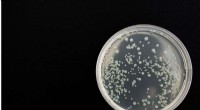
- Onderzoekers maken de weg vrij voor grootschalige, efficiënte organische zonnecellen met waterbehandeling

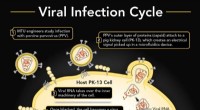
- Microfluidics helpt ingenieurs om virale infectie in realtime te bekijken
 Bioloog ontdekt wat misschien wel de 'kieskeurigste' partners ter wereld zijn
Bioloog ontdekt wat misschien wel de 'kieskeurigste' partners ter wereld zijn  Welk systeem in het lichaam bevindt zich pezen meer specifiek, zoals waar been, indien aanwezig?
Welk systeem in het lichaam bevindt zich pezen meer specifiek, zoals waar been, indien aanwezig?  Hoeveel jaar geleden was de straling die je ziet en voelt van Sun vandaag geproduceerd door nucleaire reacties in de zon?
Hoeveel jaar geleden was de straling die je ziet en voelt van Sun vandaag geproduceerd door nucleaire reacties in de zon?  Mensen vertrouwen te veel op virtuele assistenten
Mensen vertrouwen te veel op virtuele assistenten Een olievlek opruimen
Een olievlek opruimen Onderzoekers maken waterstofbrandstof uit zeewater
Onderzoekers maken waterstofbrandstof uit zeewater Tropische cycloon Trevor vult Australische Golf van Carpentaria in NASA-afbeelding
Tropische cycloon Trevor vult Australische Golf van Carpentaria in NASA-afbeelding Hoeveel uur duisternis heeft de Zuidpool op 21 juni?
Hoeveel uur duisternis heeft de Zuidpool op 21 juni?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

