
Wetenschap
Reactie van Na2S2O5 plus H2O2- en pH -effect?
Reactie van Na₂s₂o₅ met H₂o₂:
De reactie van natriummetabisulfiet (Na₂s₂o₅) met waterstofperoxide (H₂o₂) is een redoxreactie die natriumsulfaat (Na₂so₄), zwavelzuur (H₂so₄) en water (H₂o) produceert.
De algehele gebalanceerde chemische vergelijking is:
Na₂s₂o₅ + 2h₂o₂ → 2na₂so₄ + H₂so₄ + H₂o
mechanisme:
* oxidatie: H₂o₂ fungeert als een oxidatiemiddel en oxideert de zwavel in Na₂s₂o₅ van +4 tot +6.
* reductie: H₂o₂ wordt gereduceerd van -1 tot -2 en vormt water.
pH -effect:
De pH van het reactiemengsel speelt een cruciale rol in de reactiesnelheid en productvorming.
* zure pH: In zure omstandigheden wordt de reactie begunstigd, wat leidt tot de vorming van zwavelzuur als het belangrijkste product. Dit komt omdat de zure omgeving de reductie van H₂o₂ tot water bevordert en de oxidatie van na₂s₂o₅ tot na₂so₄.
* Basis pH: In basisomstandigheden wordt de reactie vertraagd en wordt de vorming van zwavelzuur onderdrukt. In plaats daarvan kan natriumsulfiet (Na₂so₃) worden gevormd als een bijproduct.
factoren die de reactie beïnvloeden:
* concentratie van reactanten: Hogere concentraties van zowel Na₂s₂o₅ als H₂o₂ zullen de reactiesnelheid verhogen.
* Temperatuur: De reactie is exotherme en het verhogen van de temperatuur zal de reactie versnellen.
* Aanwezigheid van katalysatoren: Bepaalde metaalionen, zoals ijzer of mangaan, kunnen als katalysatoren fungeren en de reactie versnellen.
Praktische toepassingen:
Deze reactie wordt in verschillende toepassingen gebruikt, waaronder:
* Pulp- en papierindustrie: Gebruikt als een bleekmiddel voor pulp en papier.
* Waterbehandeling: Gebruikt om opgelost ijzer en mangaan uit water te verwijderen.
* Voedselindustrie: Gebruikt als conserveermiddel en antioxidant.
Veiligheidsoverwegingen:
* H₂o₂ is een sterke oxidatiemiddel en kan brandwonden veroorzaken. Hanteren met zorg.
* Na₂s₂o₅ kan zwaveldioxidegas afgeven, wat giftig is. Zorg voor een goede ventilatie.
* De reactie kan exotherme zijn en warmte genereren. Gebruik passende veiligheidsmaatregelen.
Het is belangrijk om te onthouden: Deze informatie is alleen voor educatieve doeleinden en moet niet als professioneel advies worden beschouwd. Als u van plan bent deze reactie uit te voeren, raadpleeg dan altijd de relevante veiligheidsgegevensbladen en neemt u passende voorzorgsmaatregelen.
 Hoe maak je een kobaltbohr -model?
Hoe maak je een kobaltbohr -model?  Waarom vertonen lanthaniden vergelijkbaar chemisch gedrag?
Waarom vertonen lanthaniden vergelijkbaar chemisch gedrag?  Zakken of bakken? Als het om recycling gaat, is het antwoord ingewikkeld
Zakken of bakken? Als het om recycling gaat, is het antwoord ingewikkeld  Met stikstof gedoteerde koolstoflagen verhogen de efficiëntie en stabiliteit van nikkelkatalysatoren bij kamertemperatuur
Met stikstof gedoteerde koolstoflagen verhogen de efficiëntie en stabiliteit van nikkelkatalysatoren bij kamertemperatuur  Wie heeft de Nobelprijs gewonnen voor zowel natuurkunde als chemie?
Wie heeft de Nobelprijs gewonnen voor zowel natuurkunde als chemie?
 De oceaan herinnert zich:onderzoek suggereert dat de oceaan het grootste deel van de 20e eeuw een relatief constante temperatuur heeft behouden
De oceaan herinnert zich:onderzoek suggereert dat de oceaan het grootste deel van de 20e eeuw een relatief constante temperatuur heeft behouden Uit internationaal onderzoek blijkt dat onweersbuien ervoor zorgen dat het zee-ijs op de Noordpool sneller smelt
Uit internationaal onderzoek blijkt dat onweersbuien ervoor zorgen dat het zee-ijs op de Noordpool sneller smelt  Helpt het natuurbehoud door een prijs op de natuur te zetten?
Helpt het natuurbehoud door een prijs op de natuur te zetten?  Onderzoekers constateren dat bommen uit de Eerste en Tweede Wereldoorlog in de grond vluchtiger worden
Onderzoekers constateren dat bommen uit de Eerste en Tweede Wereldoorlog in de grond vluchtiger worden  Kritieke grondwatervoorraden herstellen mogelijk nooit van droogte
Kritieke grondwatervoorraden herstellen mogelijk nooit van droogte
Hoofdlijnen
- Hoeveel letters in de code voor eiwitten en hoe worden ze genoemd?
- Wetenschappers verbeteren voorspellingen over hoe de temperatuur de overlevingsvisembryo's beïnvloedt
- Zombiecellen in de zee:virussen houden de meest voorkomende mariene bacteriën onder controle
- Het belang van het bestuderen van menselijke DNA-genetica
- Het gebit van de wedgefish lijkt ontworpen om schaaldieren te pletten, maar hij eet ook pijlstaartroggen
- Wetenschappers onderzoeken hoe vrouwen hun tweede X-chromosoom afsluiten
- Wat is de PET -scan een voorbeeld van anatomische terminologie die beschrijft als een?
- Hoe noem je een kiem -expert?
- Waarom restaurants willen dat je eten bestelt op je telefoon
- Onderzoek toont aan dat het beter werken van één laag atomen op het oppervlak van een katalysator

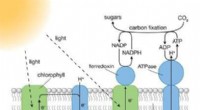
- Wetenschappers ontwerpen moleculair systeem voor kunstmatige fotosynthese
- Kleine hoeveelheden virus detecteren bij vroege infecties
- Snel en furieus:nieuwe klasse van 2D-materialen slaat elektrische energie op
- Mini-centrifuge voor eenvoudigere studie van bloedcellen opent nieuwe organ-on-chip mogelijkheden

 Nieuwe theorie suggereert dat botsing van dwergstelsels donkere materievrije sterrenstelsels zou kunnen verklaren
Nieuwe theorie suggereert dat botsing van dwergstelsels donkere materievrije sterrenstelsels zou kunnen verklaren Waar kunt u Hunt Gems rocken in Idaho
Waar kunt u Hunt Gems rocken in Idaho  Curiosity legt prachtige uitzichten vast op een veranderend Marslandschap
Curiosity legt prachtige uitzichten vast op een veranderend Marslandschap Persoonlijke koelunits in het verschiet
Persoonlijke koelunits in het verschiet In welke richting roteren planeten en ruimtelijke deeltjes rond de zon?
In welke richting roteren planeten en ruimtelijke deeltjes rond de zon?  Simulaties bieden een mogelijke verklaring voor de mysterieuze kloof in de grootteverdeling van superaardes
Simulaties bieden een mogelijke verklaring voor de mysterieuze kloof in de grootteverdeling van superaardes  Waarom heeft uw lichaam zonneschijn nodig?
Waarom heeft uw lichaam zonneschijn nodig?  Rijd met Juno terwijl hij langs de grootste maan van het zonnestelsel en Jupiter vliegt
Rijd met Juno terwijl hij langs de grootste maan van het zonnestelsel en Jupiter vliegt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

