
Wetenschap
Hoe maak je een kobaltbohr -model?
* BOHR Model Beperkingen: Het Bohr -model is een vereenvoudigde weergave van de atoomstructuur. Het werkt goed voor waterstof, maar slaagt er niet in om het gedrag van atomen met meerdere elektronen nauwkeurig weer te geven. Het kan de complexiteit van elektronenorbitalen en energieniveaus in multi-elektronenatomen zoals kobalt niet verklaren.
* Cobalt's complexiteit: Kobalt heeft 27 elektronen en is een overgangsmetaal. De elektronenconfiguratie is vrij complex met meerdere energieniveaus en orbitalen.
U kunt echter conceptueel een kobaltmodel vertegenwoordigen:
1. Nucleus: Begin met een centrale kern. Hier verblijven de protonen (27 voor kobalt) en neutronen (32 of 33 voor de twee meest voorkomende kobaltisotopen).
2. energieniveaus: Teken concentrische cirkels rond de kern om de verschillende energieniveaus (schalen) weer te geven. Voor kobalt zou je hebben:
* shell 1: 2 elektronen
* shell 2: 8 elektronen
* shell 3: 15 elektronen (inclusief de 3D -elektronen)
* shell 4: 2 elektronen
3. Elektronenverdeling: Plaats de elektronen binnen elk energieniveau. U kunt stippen of kleine cirkels gebruiken om ze te vertegenwoordigen. U kunt ze niet in specifieke orbitalen plaatsen, omdat het Bohr -model geen orbitalen weergeeft.
4. Beperkingen: Houd er rekening mee dat deze weergave uiterst vereenvoudigd is. De echte opstelling van elektronen in kobalt is veel ingewikkelder.
Overweeg in plaats van een fysiek model deze alternatieven te gebruiken:
* software: Er zijn verschillende softwareprogramma's (zoals ChemDraw of Avogadro) die 3D -visualisaties van atomen en moleculen kunnen creëren. Deze programma's kunnen de elektronenconfiguratie van kobalt nauwkeurig weergeven.
* illustraties: Zoek naar illustraties van de elektronenconfiguratie van kobalt. Deze illustraties kunnen nauwkeuriger zijn dan een eenvoudig Bohr -model.
* educatieve bronnen: Raadpleeg chemie -schoolboeken of online bronnen voor meer accurate representaties van atomaire structuur.
Vergeet niet dat het Bohr -model een waardevol hulpmiddel is voor het onderwijzen van basisconcepten over de atomaire structuur, maar het is geen perfecte weergave van de realiteit, vooral voor complexe atomen zoals kobalt.
 Wat was het belangrijkste voorstel in Charles op oorsprong van soorten?
Wat was het belangrijkste voorstel in Charles op oorsprong van soorten?  Hoe bereid je je voor op een hyperactief orkaanseizoen
Hoe bereid je je voor op een hyperactief orkaanseizoen Onderzoekers gebruiken AI om prioriteitsgebieden te definiëren voor actie om ontbossing in de Amazone tegen te gaan
Onderzoekers gebruiken AI om prioriteitsgebieden te definiëren voor actie om ontbossing in de Amazone tegen te gaan Geowetenschappers ontdekken dat ondiepe afvalwaterinjectie diepe aardbevingen in Texas veroorzaakt
Geowetenschappers ontdekken dat ondiepe afvalwaterinjectie diepe aardbevingen in Texas veroorzaakt Golven en getijden hebben een grotere impact op het leven in zee dan menselijke activiteit
Golven en getijden hebben een grotere impact op het leven in zee dan menselijke activiteit
Hoofdlijnen
- De buitenste enkele laag van een cel die elkaar overlapt als gordelroos in haar?
- Wat zijn de 2 dingen die nodig zijn om evolutie te laten plaatsvinden?
- Wat is de rol van centriolen?
- Hoe bidsprinkhaangarnalen vele vormen ontwikkelden met dezelfde krachtige stoot
- Waar wordt suiker uit het lichaam verwijderd?
- Death Valley wordt elke 10 jaar gevuld met wilde bloemen - het gebeurt nu!
- Is die schildpad legaal? Bestrijding van de handel in wilde dieren en planten met stabiele isotopen
- Wat is er anders tussen de twee soorten gisting?
- Hoe bacteriën overleven in omgevingen met weinig zuurstof
- Nieuwe, op chips gebaseerde tool voor genexpressie analyseert RNA snel en nauwkeurig

- Chemici maken de helderste fluorescerende materialen ooit

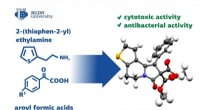
- Chemici ontwikkelen een methode om verbindingen voor geneesmiddelen te synthetiseren
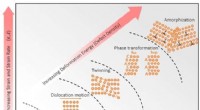
- Eilanden zonder structuur in metaallegeringen kunnen leiden tot hardere materialen
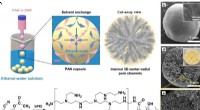
- Nieuwe technologie verhoogt de terugwinning van edele metalen uit afval drastisch
 Technische nanobodies als redders in nood wanneer SARS-CoV-2-varianten aanvallen
Technische nanobodies als redders in nood wanneer SARS-CoV-2-varianten aanvallen Onderzoekers tonen aan dat buigende halfgeleiders elektriciteit opwekken
Onderzoekers tonen aan dat buigende halfgeleiders elektriciteit opwekken De magnetische eigenschappen van stervormende dichte kernen
De magnetische eigenschappen van stervormende dichte kernen Afleveringssystemen voor deeltjesvormige vaccins kunnen helpen beschermen tegen uitbraken van infectieziekten en bioterreurbedreigingen
Afleveringssystemen voor deeltjesvormige vaccins kunnen helpen beschermen tegen uitbraken van infectieziekten en bioterreurbedreigingen Australische politie onderzoekt vermeende hackers die losgeld eisen
Australische politie onderzoekt vermeende hackers die losgeld eisen Waarom Nieuw-Zeeland terecht een beroep doet op Canada over zijn zuivelindustrie
Waarom Nieuw-Zeeland terecht een beroep doet op Canada over zijn zuivelindustrie Origins of life-onderzoekers ontwikkelen een nieuwe ecologische biosignatuur
Origins of life-onderzoekers ontwikkelen een nieuwe ecologische biosignatuur Coronavirus:waarom we een einde moeten maken aan het pandemische verbod op herbruikbare bekers
Coronavirus:waarom we een einde moeten maken aan het pandemische verbod op herbruikbare bekers
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

