
Wetenschap
Elektronenstipdiagram voor zwavel 8 molecuul?
Inzicht in de structuur
* Sulphur's Valentie -elektronen: Zwavel heeft 6 valentie -elektronen.
* octetregel: Zwavelatomen delen meestal elektronen om een stabiel octet te bereiken (8 valentie -elektronen).
* S8 -structuur: In het S8-molecuul vormen de zwavelatomen een kroonvormige ring waarbij elk zwavelatoom wordt gebonden aan twee andere zwavelatomen.
Representatie van elektronendiagram Diagram
Helaas vertegenwoordigt een traditioneel elektronenstotdiagram niet volledig de 3D -structuur van S8. Hier is een vereenvoudigde weergave die zich richt op de binding:
1. Begin met het zwavelatoom: Vertegenwoordig elk zwavelatoom met zijn symbool (en) omgeven door zes stippen die zijn valentie -elektronen vertegenwoordigen:
`` `
..
:S:
..
`` `
2. Bondvorming: Elk zwavelatoom vormt twee enkele bindingen met twee andere zwavelatomen. Deze bindingen worden weergegeven door paren stippen tussen zwavelatomen te delen.
`` `
.. ..
:S:..:s:
.. ..
`` `
3. de ring aansluiten: Dit patroon gaat verder rond de ring en vormt een gesloten ketting:
`` `
.. ..
..:S:..:S:..
.. .. ..
:S:..:s:..:s:
.. .. ..
.. ..
`` `
belangrijke opmerkingen
* Dit is een vereenvoudigde weergave, geen precieze 3D -model.
* De echte structuur van S8 heeft de zwavelatomen gerangschikt in een gepuckte, kroonvormige ring.
* Elektronenstipdiagrammen worden voornamelijk gebruikt voor eenvoudige moleculen. Meer complexe moleculen zoals S8 worden vaak weergegeven met meer gedetailleerde structurele formules.
Laat het me weten als je nog vragen hebt!
 Wat gebeurt er als een atoom een ion vormt?
Wat gebeurt er als een atoom een ion vormt?  Heeft waterschaarste invloed op productiebedrijven om de giftige uitstoot te verminderen?
Heeft waterschaarste invloed op productiebedrijven om de giftige uitstoot te verminderen?  Zoetheid voelen op moleculair niveau
Zoetheid voelen op moleculair niveau Worden Napthaleen -bal opgelost in water?
Worden Napthaleen -bal opgelost in water?  Wetenschappers ontwerpen nieuwe metabole technologie om wetenschappelijke gegevens voor iedereen te openen
Wetenschappers ontwerpen nieuwe metabole technologie om wetenschappelijke gegevens voor iedereen te openen
Hoofdlijnen
- Wat is een voorbeeld van meercellige organismen?
- Wat zijn enkele voorbeelden van een vergelijkend wetenschappelijk onderzoeksproject in de biologie?
- Wat zijn voor belangrijke soorten lymfocyten?
- Wormsoorten verloren 7, 000 genen na evolutie om zichzelf te bevruchten
- Wat is geheugenverlies precies?
- Moedigt het benoemen van gedrag mensen aan om het te doen? Een nieuwe studie zegt van wel
- Als de somatische cel 30 chromosomen heeft, hoeveel zitten er dan in de gameten?
- Welk type weefsel heeft een apicaal en basaal oppervlak?
- Welk bewijsmateriaal gebruiken wetenschappers om fylogenetische bomen te maken?
- Een eenvoudigere manier om B-cellen en T-cellen te differentiëren
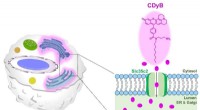
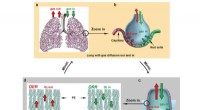
- Een op de longen geïnspireerd ontwerp verandert water in brandstof
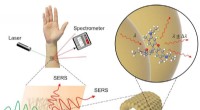
- Een nieuwe Raman chemische sensor gemaakt van noedelachtige draden van goud
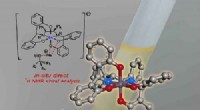
- Chemici leren een enzym een nieuwe truc, met potentieel voor het bouwen van nieuwe moleculen

- Op gallium gebaseerd oplosmiddel analyseert efficiënt optisch actieve alcoholen
 Herontdekte Apollo-gegevens geven een eerste indicatie van hoe snel maanstof zich opstapelt
Herontdekte Apollo-gegevens geven een eerste indicatie van hoe snel maanstof zich opstapelt  Hoeveel eenheden zijn er bij motoreenheid nodig om het gewicht van 160 en 80 te verhogen?
Hoeveel eenheden zijn er bij motoreenheid nodig om het gewicht van 160 en 80 te verhogen?  King Cobra Snake Feiten
King Cobra Snake Feiten  Hoe reageren bacteriegemeenschappen in zwarte bodems op conventionele en biologisch afbreekbare microplastics?
Hoe reageren bacteriegemeenschappen in zwarte bodems op conventionele en biologisch afbreekbare microplastics? Wat is NASO -compound?
Wat is NASO -compound?  8 planeten in het zonnestelsel?
8 planeten in het zonnestelsel?  Waar komen de zonnen warmte en licht vandaan?
Waar komen de zonnen warmte en licht vandaan?  Omdat microscopisch kleine materialen zich steeds vaker verspreiden, is het een prioriteit om ervoor te zorgen dat ze veilig zijn
Omdat microscopisch kleine materialen zich steeds vaker verspreiden, is het een prioriteit om ervoor te zorgen dat ze veilig zijn
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

