
Wetenschap
Wat is essentieel bij het schrijven van de chemische formule voor anorganisch zout?
1. Identificeer de kationen en anionen
* kationen: Positief geladen ionen (metalen of ammonium, NH₄⁺).
* anionen: Negatief geladen ionen (niet -metalen, polyatomische ionen).
* Voorbeeld: In NaCl (natriumchloride) is Na⁺ het kation en CL⁻ is het anion.
2. Bepaal de ladingen
* metalen: Gebruik het periodiek systeem om de gemeenschappelijke lading te bepalen. Groep 1 metalen (Li, Na, K) hebben bijvoorbeeld een +1 lading en groep 2 metalen (BE, MG, CA) hebben een +2 lading.
* niet -metalen: Deze hebben meestal een vaste negatieve lading op basis van hun positie op de periodieke tabel (halogenen zoals CL, BR, ik heb een -1 lading).
* Polyatomische ionen: Onthoud de gemeenschappelijke polyatomische ionen en hun ladingen (bijv. Sulfaat So₄²⁻, fosfaat po₄³⁻, nitraat NO₃⁻).
3. Het balanceren van de ladingen
* De totale positieve lading moet gelijk zijn aan de totale negatieve lading.
* eenvoudige zouten:
* Als de ladingen gelijk en tegengesteld zijn, schrijf dan de symbolen naast elkaar. NA⁺ en CL⁻ combineren bijvoorbeeld om NaCl te vormen.
* Als de kosten niet gelijk zijn, gebruik dan subscripties om het aantal van elk ion aan te geven dat nodig is om de kosten in evenwicht te brengen. Ca²⁺ en CL⁻ combineren bijvoorbeeld om CACL₂ te vormen (één calciumionen balanceert twee chloride -ionen).
* Complexe zouten:
* Gebruik haakjes om polyatomische ionen om te sluiten als ze meer dan eens verschijnen. Bijvoorbeeld (NH₄) ₂SO₄ (ammoniumsulfaat).
* Soms is een Romeins cijfer nodig in de naam om de lading van het metaalkation (bijv. IJzer (ii) chloride, fecl₂) aan te geven.
4. De formule schrijven
* Plaats eerst het kationsymbool, gevolgd door het anionsymbool.
* Gebruik subscripts om het nummer van elk ion aan te geven dat nodig is voor ladingsaldo.
* Voorbeeld:
* Magnesiumbromide:mg²⁺ en br⁻ -> mgbr₂
* Kaliumfosfaat:k⁺ en po₄³⁻ -> k₃po₄
5. Het vereenvoudigen van de formule
* Gebruik altijd de eenvoudigste ratio van ionen van het hele nummer.
belangrijke opmerkingen
* naamgeving: Leer de regels voor het benoemen van anorganische zouten. De meeste binaire zouten (twee elementen) gebruiken bijvoorbeeld de naam van het metaal gevolgd door het niet-metaal met "-ide" aan het einde.
* Periodieke tabel: Gebruik het periodiek systeem als uw primaire hulpbron om ladingen en gemeenschappelijke oxidatietoestanden van elementen te bepalen.
* Oefening: Hoe meer je oefent om formules te schrijven, hoe comfortabeler je wordt met het proces.
Laat het me weten als je voorbeelden wilt of specifieke zouten hebt waarvoor je wilt proberen formules te schrijven!
 Heeft het wonen in de buurt van een olie- of aardgasbron invloed op uw drinkwater?
Heeft het wonen in de buurt van een olie- of aardgasbron invloed op uw drinkwater?  Waarom wordt niet verwacht dat CaO reageert met natriumhydroxide?
Waarom wordt niet verwacht dat CaO reageert met natriumhydroxide?  Hoe zout uit water te halen:laat het zelf uitwerpen
Hoe zout uit water te halen:laat het zelf uitwerpen Kunnen huizen van de toekomst gemaakt worden door bacteriën?
Kunnen huizen van de toekomst gemaakt worden door bacteriën? Verdubbelt het verdubbelen van de zuur- en baseconcentraties in een neutralisatiereactie de hoeveelheid warmte die vrijkomt?
Verdubbelt het verdubbelen van de zuur- en baseconcentraties in een neutralisatiereactie de hoeveelheid warmte die vrijkomt?
Hoofdlijnen
- Gedragsstudies tonen aan dat bavianen en duiven in staat zijn tot cognitie op een hoger niveau
- Hoe worden micro -organismen gebruikt om Quorn te maken?
- Karkas van Noord-Atlantische rechtse walvis gespot in Massachusetts
- Wat wordt bedoeld met de term menselijke genenpool?
- Waarom S-gekoppelde glycosylatie de rol van natuurlijke O-glycosylatie niet adequaat kan nabootsen
- Reproductieproces bij mensen
- Biologen laten zien hoe de evolutie van fysieke eigenschappen gedrag kan beïnvloeden
- Is in een wetenschappelijk experimentbeheersing daarvan het onderdeel?
- Welke factoren zijn belangrijk voor classificatie?
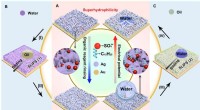
- Elektrolytisch gedeponeerde oppervlakken met omkeerbaar schakelende grensvlakeigenschappen
- Organische elektronica:een nieuwe halfgeleider in de koolstofnitride-familie

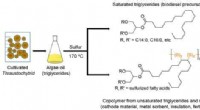
- Eenvoudige methode om hoogwaardige bioactieve stoffen te extraheren uit eencellige algenolie
- Wetenschappers stellen nieuwe selectieve reductieve aminekatalysatoren voor met verbeterde stabiliteit

- Wetenschappers ontwikkelen moleculaire code voor melanine-achtige materialen

 Studie:Slechts 1 op de 5 mensen met een beperking werkt vanuit huis; miljoenen hebben nog steeds geen optie
Studie:Slechts 1 op de 5 mensen met een beperking werkt vanuit huis; miljoenen hebben nog steeds geen optie Wat zijn de fysieke eigenschappen van parel?
Wat zijn de fysieke eigenschappen van parel?  Waarom zorg je ervoor dat je handen droog zijn bij het gebruik van elektrische apparatuur?
Waarom zorg je ervoor dat je handen droog zijn bij het gebruik van elektrische apparatuur?  Feiten over Australische woestijnen
Feiten over Australische woestijnen  Het magnetische lied van de aarde voor het eerst opgenomen tijdens een zonnestorm
Het magnetische lied van de aarde voor het eerst opgenomen tijdens een zonnestorm Hoeveel kernelektronen zijn er in Germanium?
Hoeveel kernelektronen zijn er in Germanium?  Houd niet van:Facebook gaat in beroep tegen Duitse uitspraak over datagebruik
Houd niet van:Facebook gaat in beroep tegen Duitse uitspraak over datagebruik Waarom zijn sommige E. coli dodelijk terwijl andere vreedzaam in ons lichaam leven?
Waarom zijn sommige E. coli dodelijk terwijl andere vreedzaam in ons lichaam leven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

