
Wetenschap
De koolstofatomen in grafiet en de diamant hebben anders?
Hier is een uitsplitsing:
* grafiet: Koolstofatomen in grafiet zijn gerangschikt in platte vellen van zeshoekige ringen, zoals een honingraatstructuur. Binnen elk vel worden de koolstofatomen verbonden door sterke covalente bindingen. De lakens zelf worden echter bij elkaar gehouden door zwakke Van der Waals Forces. Deze zwakke verbindingsbinding maakt grafiet zacht, glad en een goede geleider van elektriciteit.
* diamant: Koolstofatomen in diamant zijn gerangschikt in een driedimensionaal tetraëdrisch netwerk, waarbij elk koolstofatoom vier sterke covalente bindingen vormt. Deze rigide, onderling verbonden structuur maakt diamant uitzonderlijk hard, met een hoog smeltpunt en een slechte geleider van elektriciteit.
Samenvattend: Het verschil in de bindingsstructuur tussen de koolstofatomen in grafiet en diamant leidt tot de volgende verschillen in hun eigenschappen:
* Hardheid: Diamond is het moeilijkst bekende natuurlijke materiaal, terwijl grafiet zacht is en gemakkelijk kan worden bekrast.
* elektrische geleidbaarheid: Grafiet is een goede geleider van elektriciteit, terwijl Diamond een slechte geleider is.
* smeltpunt: Diamond heeft een veel hoger smeltpunt dan grafiet.
* uiterlijk: Diamant is transparant, terwijl grafiet zwart en ondoorzichtig is.
 Eerste betrouwbare schattingen van zeer radioactieve cesiumrijke microdeeltjes die vrijkomen bij de ramp in Fukushima
Eerste betrouwbare schattingen van zeer radioactieve cesiumrijke microdeeltjes die vrijkomen bij de ramp in Fukushima Rusland lanceert gigantisch Yamal-gasproject in het noordpoolgebied
Rusland lanceert gigantisch Yamal-gasproject in het noordpoolgebied Hoe ziet het Freesia -blad eruit?
Hoe ziet het Freesia -blad eruit?  Total onthult belangrijke offshore gasvondst in Zuid-Afrika
Total onthult belangrijke offshore gasvondst in Zuid-Afrika Diversiteit is de sleutel tot duurzaamheid voor de lokale kippenhouderij in Afrika
Diversiteit is de sleutel tot duurzaamheid voor de lokale kippenhouderij in Afrika
Hoofdlijnen
- Wat wordt bedoeld met fysiologische acidose als de pH van het bloed tussen 7 en 7,35 ligt?
- Kan een bacteriën leven zonder zijn gastheer?
- Wat is ventilatie in de menselijke biologie?
- Wat zijn de 3 principes van de celtheorie?
- Waarom is het belangrijk dat voedingsstoffen snel het centrum van een cel bereiken?
- Wat is het diafragma van op een microscoopcontrole?
- In welk type cellen resulteert mitose?
- Wat zijn twee algemene categorieën die er toe doen, kunnen worden geclassificeerd?
- Nieuwe technologie verlicht microben die niet in een laboratorium kunnen worden gekweekt
- Heeft komeetinslagen het leven op aarde een boost gegeven?

- Flexibele thermo-elektrische generatormodule:een wondermiddel om problemen met afvalenergie op te lossen

- Niet alleen brood en bier:microben kunnen koolstofdioxide fermenteren om ook brandstof te maken
- Waterstofproductie in een besloten ruimte
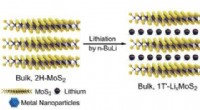
- Nieuw bioremediatiemateriaal kan chemicaliën voor altijd reinigen

 Is de Euphrates een Afrikaanse rivier?
Is de Euphrates een Afrikaanse rivier?  Hoe verschijnt er een hemelse object wanneer het dichter bij de kijker komt?
Hoe verschijnt er een hemelse object wanneer het dichter bij de kijker komt?  Dragcultuur is misschien mainstream, maar zijn vormen evolueren voortdurend
Dragcultuur is misschien mainstream, maar zijn vormen evolueren voortdurend Wat kan 20 mol natriumchloride maken?
Wat kan 20 mol natriumchloride maken?  Waarom lijken circumpolaire sterren nooit onder de horizon te gaan?
Waarom lijken circumpolaire sterren nooit onder de horizon te gaan?  Studie:Virussen ondersteunen fotosynthese in bacteriën – een evolutionair voordeel?
Studie:Virussen ondersteunen fotosynthese in bacteriën – een evolutionair voordeel?  Gas onder druk zetten
Gas onder druk zetten Federale studie vindt ras, geslacht beïnvloedt gezichtsscantechnologie
Federale studie vindt ras, geslacht beïnvloedt gezichtsscantechnologie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

