
Wetenschap
Van chlooratomen wordt gezegd dat ze de vernietiging van stratosferische ozon katalyseren omdat?
1. Initiatie: Een chlooratoom (CL) ontmoet een ozonmolecuul (O 3 ).
2. reactie: Het chlooratoom trekt een zuurstofatoom uit ozon en vormt chloormonoxide (CLO) en moleculaire zuurstof (O 2 ):
`` `
Cl + O 3 → clo + o 2
`` `
3. kettingpropagatie: De clo ontmoet vervolgens een vrij zuurstofatoom (O), dat overvloedig is in de stratosfeer vanwege de splitsing van ozon door UV -straling:
`` `
Clo + o → cl + o 2
`` `
4. Regeneratie: Het chlooratoom wordt in deze stap geregenereerd en kan nu teruggaan naar stap 1, waardoor de cyclus wordt herhaald.
De belangrijkste punten:
* katalytisch: Het chlooratoom wordt in het proces niet geconsumeerd, maar fungeert als een katalysator, waardoor veel ozonmoleculen worden vernietigd.
* kettingreactie: De cyclus gaat door zolang chlooratomen aanwezig zijn, wat leidt tot een snelle uitputting van ozon.
* Ozon -uitputting: Elk chlooratoom kan duizenden ozonmoleculen vernietigen voordat het uiteindelijk uit de stratosfeer wordt verwijderd.
Waarom dit een probleem is:
Ozon in de stratosfeer werkt als een schild en absorbeert schadelijke ultraviolette (UV) straling van de zon. De uitputting ervan maakt het mogelijk om meer UV -straling het aardoppervlak te bereiken, waardoor het risico op huidkanker, staar en andere gezondheidsproblemen toeneemt.
Belangrijke opmerking: De belangrijkste bron van chlooratomen in de stratosfeer was chlorofluorocoolwaterstoffen (CFC's), die ooit op grote schaal werden gebruikt in koelmiddelen, aerosolen en andere producten. Vanwege internationale overeenkomsten zoals het Montreal -protocol is het gebruik van CFC's drastisch verminderd, wat leidt tot een geleidelijk herstel van de ozonlaag.
 Wat is de conclusie van krijt als alternatief voor vloeibare gum?
Wat is de conclusie van krijt als alternatief voor vloeibare gum?  Wat is de formule voor het geconjugeerde zuur van CH3COO-?
Wat is de formule voor het geconjugeerde zuur van CH3COO-?  Wat is het gebruik van ioniserende straling?
Wat is het gebruik van ioniserende straling?  Waarom kan een mengsel geen unieke chemische formule hebben?
Waarom kan een mengsel geen unieke chemische formule hebben?  Onzichtbaar, rekbare circuits om de volgende generatie technologie vorm te geven
Onzichtbaar, rekbare circuits om de volgende generatie technologie vorm te geven
 Verschil tussen natuurlijke selectie en afstamming met wijziging
Verschil tussen natuurlijke selectie en afstamming met wijziging  Fossiele brandstoffen zijn slecht voor je gezondheid en schadelijk in veel opzichten naast klimaatverandering
Fossiele brandstoffen zijn slecht voor je gezondheid en schadelijk in veel opzichten naast klimaatverandering Wanneer zou een levenswetenschapper niet-levende dingen zoals een meer of een rots bestuderen?
Wanneer zou een levenswetenschapper niet-levende dingen zoals een meer of een rots bestuderen?  Hoe kunt u de netheid van ons landwater en lucht heipten?
Hoe kunt u de netheid van ons landwater en lucht heipten?  UNESCO dringt er bij Polen op aan te stoppen met het kappen van oerbos
UNESCO dringt er bij Polen op aan te stoppen met het kappen van oerbos
Hoofdlijnen
- Welk onderwerp wordt de vader van alle wetenschappen genoemd?
- Studies leveren een beter begrip op van hoe cyanobacteriën voordeel halen uit glucose
- Wat is de symbiotische relatie tussen mug en mensen?
- Wat zijn de drie belangrijkste wetenschapsgroepen?
- Wat veroorzaakt slaap? Bij fruitvliegjes is het stress op cellulair niveau
- Eiwitten in haaientanden kunnen een aanwijzing zijn voor wat ze eten
- Hoe ondersteunen fossiele en biochemicaliën de evolutietheorie?
- Hoe een moleculair 'alarm'-systeem planten beschermt tegen roofdieren
- Wat zijn 3 mechanismen en aanpassingen voor zaadverspreiding?
- Sleutelenzym dat in planten wordt aangetroffen, kan de ontwikkeling van medicijnen en andere producten leiden
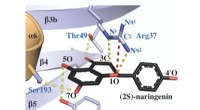
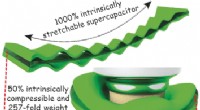
- Superrekbaar, supercompressibele supercondensatoren
- In het laboratorium gemaakte eiwit chomps co-factor als een grote ol gator
- Efficiëntiesprong bij het scheiden van para-xyleen met behulp van nieuwe koolstofmembranen

- Op maat gemaakte enzymatische oplossingen verminderen de tijd en kosten van bioraffinageprocessen

 Waarom lijken sommige sterren helderder dan anderen de temperatuur of grootte?
Waarom lijken sommige sterren helderder dan anderen de temperatuur of grootte?  Hoe verbeteren de efficiëntie van de kookplaat?
Hoe verbeteren de efficiëntie van de kookplaat?  Hoe zou u de Constellation Orion beschrijven?
Hoe zou u de Constellation Orion beschrijven?  Nieuwe sensortechnologie kan bloedonderzoek bij COVID-patiënten versnellen
Nieuwe sensortechnologie kan bloedonderzoek bij COVID-patiënten versnellen Netflix-effect:Snoersnijden versnelt op Amerikaanse markt
Netflix-effect:Snoersnijden versnelt op Amerikaanse markt Waarom staat endoskelet toe dat gewervelde dieren groter worden dan dieren zonder endoskeletten?
Waarom staat endoskelet toe dat gewervelde dieren groter worden dan dieren zonder endoskeletten?  Wat is 44.8c in Fahrenheit?
Wat is 44.8c in Fahrenheit?  Wat is de breedte van ons zonnestelsel?
Wat is de breedte van ons zonnestelsel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

