
Wetenschap
De geometrie van een waterstofbromidemolecuul is wat?
Dit is waarom:
* Structuur: HBR bestaat uit één waterstofatoom en één broomatoom.
* binding: Het waterstofatoom deelt zijn enkele elektron met het broomatoom en vormt een enkele covalente binding.
* elektronenparen: Het broomatoom heeft zeven valentie -elektronen, waarbij één betrokken is bij de binding met waterstof. Dit laat drie eenzame paren elektronen rond het broomatoom achter.
* afstoting: De eenzame paren elektronen op broom brengen afstoting uit op de H-BR-binding en duwen het waterstofatoom zo ver mogelijk weg.
* lineaire geometrie: Deze afstoting leidt tot een lineaire geometrie waarbij het waterstofatoom en broomatoom aan weerszijden van het broomatoom worden geplaatst, waardoor een rechte lijn ontstaat.
 Wat herstelt ionische omstandigheden en welke elektrische omstandigheden?
Wat herstelt ionische omstandigheden en welke elektrische omstandigheden?  Hoeveel totale valentie -elektronen zijn er in het zwembad voor fosfor trifluoride?
Hoeveel totale valentie -elektronen zijn er in het zwembad voor fosfor trifluoride?  Nieuwe oplosmiddelen om plantaardige cellulose af te breken voor bio-ethanol
Nieuwe oplosmiddelen om plantaardige cellulose af te breken voor bio-ethanol Herontworpen enzym kan schade door ruggenmergletsel en beroerte helpen terugdraaien
Herontworpen enzym kan schade door ruggenmergletsel en beroerte helpen terugdraaien Welke grondstoffen van olie en aardgas?
Welke grondstoffen van olie en aardgas?
Hoofdlijnen
- Reproductie waar is er maar één ouder?
- Noem de Tubluar -klieren die worden gevonden tussen bases van darmvilli?
- Experiment laat zien hoe massale sterfte door roofdieren de voedselwebben beïnvloedt
- Wiskundig model verklaart waarom sommige bacteriën zelfs in kleine doses ziekten veroorzaken
- Hoe zijn voorvoegsels nuttig in de wetenschap?
- Wat zijn de structuur en functie van het ciliated epitheel?
- Gevlekte lantaarnvliegen komen weer uit. Maar hoe ver verspreiden ze zich elk jaar?
- Wetenschappers onthullen hoe de biologische activiteit wordt gereguleerd in fruitvlieg- en rondwormgenomen
- Hoe MRNA naar TRNA
- Onderzoekers observeren organische chemische reactie met elektronenmicroscoop

- Milieuvriendelijk kooldioxide-conversieproces kan een revolutie teweegbrengen in de bestaande methode

- Paradigmaverschuivende theorie benadrukt het belang van substraatflexibiliteit in enzymatische reacties

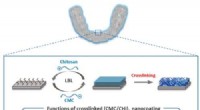
- Tandhouders en aligners helpen om bacteriën te bestrijden
- Innovatiepioniers scoren wereldprimeur voor duurzaam bouwen met grafeenbeton

 Simpele modellen voor projecten voor het broeikaseffect van de aarde
Simpele modellen voor projecten voor het broeikaseffect van de aarde  Over het algemeen kan een polair oplosmiddel geen opgeloste stof oplossen?
Over het algemeen kan een polair oplosmiddel geen opgeloste stof oplossen?  Wat is het doel van hybridisatie?
Wat is het doel van hybridisatie?  Wat is de potentiële energie in joules van een massa van 100 kg 10 meter boven de grond?
Wat is de potentiële energie in joules van een massa van 100 kg 10 meter boven de grond?  Waarom kunnen we ons niet herinneren dat we baby's waren?
Waarom kunnen we ons niet herinneren dat we baby's waren?  Is het waar dat één bioom kan bestaan uit gebieden over de hele wereld, hetzelfde klimaat en organismen hebben?
Is het waar dat één bioom kan bestaan uit gebieden over de hele wereld, hetzelfde klimaat en organismen hebben?  De grootste bomen vangen de meeste koolstof op:grote bomen domineren de koolstofopslag in bossen
De grootste bomen vangen de meeste koolstof op:grote bomen domineren de koolstofopslag in bossen Het printen van circuits op zeldzame nanomagneten geeft een nieuwe draai aan computergebruik
Het printen van circuits op zeldzame nanomagneten geeft een nieuwe draai aan computergebruik
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

