
Wetenschap
Welke elementen gevonden in de vrije elementaire staat?
elementen die vaak worden gevonden in hun vrije elementaire toestand
* Nobele gassen: Helium (HE), Neon (NE), Argon (AR), Krypton (KR), Xenon (XE), Radon (RN) - Deze zijn zeer niet -reactief en bestaan als enkele atomen.
* Sommige niet -metalen:
* Waterstof (H2) - bestaat als een diatomisch gas.
* Stikstof (N2) - Bestaat als een diatomee -gas.
* Zuurstof (O2) - Bestaat als een diatomee -gas.
* Zwavel (S8) - Gevonden als een vaste stof in de vorm van de octatomische allotrope (S8).
* Fosfor (P4) - bestaat als een vaste stof in de vorm van de tetratomische allotrope (P4).
* Sommige metalen:
* Goud (AU) - Zeer niet -reactief en vaak gevonden in zijn inheemse vorm.
* Silver (Ag) - Relatief niet -reactief en vaak gevonden in zijn inheemse vorm.
* Platina (PT) - Zeer niet -reactief en vaak gevonden in zijn inheemse vorm.
* Koper (Cu) - kan worden gevonden in zijn inheemse vorm, maar het is gebruikelijker om het in ertsen te vinden.
Waarom deze elementen worden gevonden in hun vrije staat:
* Lage reactiviteit: Nobele gassen en sommige niet -metalen zijn zeer niet -reactief vanwege hun stabiele elektronenconfiguraties. Ze vormen niet gemakkelijk banden met andere elementen.
* Ongewone reacties: Sommige metalen zoals goud, zilver en platina zijn zeer niet -reactief en resistent tegen corrosie.
* Natuurlijke overvloed: Elementen zoals waterstof, stikstof en zuurstof zijn overvloedig in de atmosfeer.
belangrijke opmerkingen:
* allotropen: Elementen zoals zwavel, fosfor en koolstof kunnen bestaan in verschillende vormen die allotropen worden genoemd (bijv. Diamant, grafiet en fullereen zijn allotropen van koolstof).
* zeldzame gevallen: Hoewel de hierboven genoemde elementen vaak worden gevonden in hun vrije toestanden, kunnen sommige ook bestaan in verbindingen.
* Elementaire toestand versus geïsoleerd: Het feit dat een element in zijn vrije staat wordt gevonden, betekent niet dat het volledig geïsoleerd is. Het kan bestaan in een mengsel met andere elementen.
Laat het me weten als je nog meer vragen hebt!
 Waarom waren de branden in de wijnlanden van Californië zo verwoestend?
Waarom waren de branden in de wijnlanden van Californië zo verwoestend?  Maken wolven het moeilijker om herten op aas te jagen?
Maken wolven het moeilijker om herten op aas te jagen?  Hoe het bestuderen van (robot)duivennavigatie mijn mening over hun intellect veranderde
Hoe het bestuderen van (robot)duivennavigatie mijn mening over hun intellect veranderde  Freud en Oedipus:doet een van beide er nog toe?
Freud en Oedipus:doet een van beide er nog toe?  Welke planten zijn kleiner dan de aarde?
Welke planten zijn kleiner dan de aarde?
Hoofdlijnen
- Het sluiten van wegen gaat de effecten van habitatverlies voor grizzlyberen tegen
- Zouden slaaphaaien op beschermde Steller-zeeleeuwen kunnen jagen?
- Een organisme dat uit één cel bestaat, heeft geen kern?
- Hoe ademen vogels beter? De ontdekking van onderzoekers zal je voor de gek houden
- Het belang van samengestelde microscopen
- Wat zijn de attributen van levende organismen?
- Wat betekent pH voor biologie?
- Hoe zijn bloemen vergelijkbaar met de voortplantingsorganen van de plant?
- 1. Welke fundamentele levensprocessen moeten alle eencellige organismen uitvoeren om te overleven?
- Een gepatenteerde oplossing voor het verlichten van droge mond en de ontwikkeling van voedingsproducten
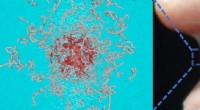
- Bloed en zweet:draagbare medische sensoren krijgen een grote gevoeligheidsboost
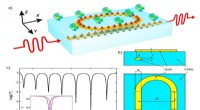
- Klein volume, organische synthese met hoge doorvoer
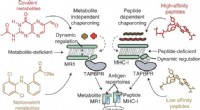
- Onderzoekers ontdekken moleculaire basis van antigeenverwerking voor kankerdoelwit MR1
- Nieuwe theorieën en materialen helpen de overgang naar schone energie

 Wat zijn fossle brandstoffen?
Wat zijn fossle brandstoffen?  Zou het mogelijk zijn om een volle maan te zien tijdens daglichturen?
Zou het mogelijk zijn om een volle maan te zien tijdens daglichturen?  Reactieresultaten voorspellen:machines leren scheikunde
Reactieresultaten voorspellen:machines leren scheikunde Welke manier kunnen wetenschappers echt van koper in goud veranderen?
Welke manier kunnen wetenschappers echt van koper in goud veranderen?  Italië vertelt Ryanair, Wizz Air stopt met opladen van bagage
Italië vertelt Ryanair, Wizz Air stopt met opladen van bagage Interne waakhond zegt dat EPA het opruimen van giftige sites verkeerd beheert
Interne waakhond zegt dat EPA het opruimen van giftige sites verkeerd beheert Wanneer zullen kunstmatige moleculaire machines voor ons gaan werken?
Wanneer zullen kunstmatige moleculaire machines voor ons gaan werken?  Een jaar later weten we nu waarom de Tongaanse uitbarsting zo gewelddadig was. Het is een wake-up call om naar andere onderzeese vulkanen te kijken
Een jaar later weten we nu waarom de Tongaanse uitbarsting zo gewelddadig was. Het is een wake-up call om naar andere onderzeese vulkanen te kijken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

