
Wetenschap
Welke temperatuur verandert vloeibaar chloor tot gas?
Vloeibare chloor heeft geen specifieke temperatuur waar deze in gas verandert. In plaats daarvan kookt het Bij een specifieke temperatuur, en dit kookpunt hangt af van de druk.
Dit is waarom:
* kookpunt: Het kookpunt is de temperatuur waarbij een vloeistof verandert in een gas.
* Druk: De druk rond de vloeistof beïnvloedt zijn kookpunt. Hogere druk maakt het moeilijker voor de vloeistof om in een gas te veranderen, zodat het kookpunt toeneemt. Lagere druk maakt het eenvoudiger, dus het kookpunt neemt af.
Bij standaard atmosferische druk (1 atmosfeer) kookt vloeibaar chloor bij -34.05 ° C (-29,29 ° F).
Dus, hoewel vloeibaar chloor niet alleen "in gas" op een specifieke temperatuur kookt, kookt het en wordt het gasvormig bij -34,05 ° C onder standaard atmosferische druk.
 Welke koninkrijken zijn heterotrofisch en autotroof?
Welke koninkrijken zijn heterotrofisch en autotroof?  Waar groeien Epiganea Repens?
Waar groeien Epiganea Repens?  Bedrijfsgeheim over klimaatverandering als doelwit van Washington en Californië
Bedrijfsgeheim over klimaatverandering als doelwit van Washington en Californië Klimaatverandering duwt Nieuw-Zeeland de warmste geregistreerde winter in
Klimaatverandering duwt Nieuw-Zeeland de warmste geregistreerde winter in Onderzoekers identificeren kenmerken van de afvoer van smeltwater in drie deelstroomgebieden van het stroomgebied van de Urumqi
Onderzoekers identificeren kenmerken van de afvoer van smeltwater in drie deelstroomgebieden van het stroomgebied van de Urumqi
Hoofdlijnen
- Puin van de tsunami van 2011 bracht honderden soorten over de Stille Oceaan
- Wat is nephoning en waarom hebben de officiële tests dit niet opgepikt?
- Waarom classificeren wetenschappers een spons als eenvoudig dier en geen plant?
- Hoe bacteriën omgaan met stress
- Welke plant bevat zowel mannelijke als vrouwelijke reproductieve structuren?
- Studie:Net als een boom laten jaarringen de leeftijd van de kreeft zien
- Wat is de vloeistof die de ruimte tussen de kern en het celmembraan vult?
- Geen leveringen:hoe cellen beslissen wanneer ze extracellulaire pakketten accepteren
- Kunnen mechanismen die tijdens de winterslaap worden gebruikt, dieren helpen nieuwe habitats te koloniseren?
- Geheime berichten verborgen in lichtgevoelige polymeren
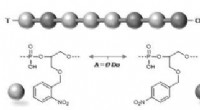
- Nieuwe ID-foto's van geleidende polymeren ontdekken een verrassende ABBA-fan

- Niet alleen brood en bier:microben kunnen koolstofdioxide fermenteren om ook brandstof te maken
- Bioactieve papiercoatings ter vervanging van plastic voor het verpakken van voedsel

- Catalyst Advance verbetert de technologie voor het reinigen van aardgas

 Hoe betrouwbaarheidsniveaus te berekenen
Hoe betrouwbaarheidsniveaus te berekenen  Wetenschappers denken dat ze de cruciale ingrediënten voor een winnend voetbalteam hebben ontdekt
Wetenschappers denken dat ze de cruciale ingrediënten voor een winnend voetbalteam hebben ontdekt Welk type energie is koppel?
Welk type energie is koppel?  Wereldrecord:plasmaversneller werkt de klok rond
Wereldrecord:plasmaversneller werkt de klok rond Energievrij supersnel computergebruik uitgevonden door wetenschappers met behulp van lichtpulsen
Energievrij supersnel computergebruik uitgevonden door wetenschappers met behulp van lichtpulsen Wat wordt door de dirigent gebruikt om synfonie te leiden?
Wat wordt door de dirigent gebruikt om synfonie te leiden?  Kleine NASA-satellieten kunnen orkaanvoorspellingen ondersteunen met GPS
Kleine NASA-satellieten kunnen orkaanvoorspellingen ondersteunen met GPS Welk percentage rotsen is metamorf sedimentair of stolling?
Welk percentage rotsen is metamorf sedimentair of stolling?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

