
Wetenschap
Waarom worden watermoleculen aangetrokken tot natriumchloor?
* polariteit: Watermoleculen (H₂o) zijn polair. Dit betekent dat ze een enigszins positief uiteinde hebben (waterstofatomen) en een enigszins negatief uiteinde (zuurstofatoom).
* ionische aard van NaCl: Natriumchloride is een ionische verbinding. Het bestaat als een kristalrooster waar natriumionen (Na⁺) positief geladen zijn en chloride -ionen (CL⁻) negatief worden geladen.
* Attractie: Het positieve uiteinde van watermoleculen (waterstof) wordt aangetrokken door de negatieve chloride -ionen, terwijl het negatieve uiteinde van watermoleculen (zuurstof) wordt aangetrokken door de positieve natriumionen. Deze aantrekkingskracht staat bekend als elektrostatische aantrekkingskracht .
Hoe het werkt:
Wanneer natriumchloride in water wordt opgelost, omringen de watermoleculen de ionen en trekken ze effectief uit elkaar. Dit komt omdat de aantrekkingskracht tussen de watermoleculen en de ionen sterker is dan de aantrekkingskracht tussen de ionen zelf.
Dit proces wordt hydratatie genoemd , en het is wat natriumchloride (tafelzout) oplosbaar maakt in water.
Samenvattend worden watermoleculen aangetrokken tot natriumchloride vanwege de elektrostatische aantrekking tussen de polaire watermoleculen en de geladen ionen van natriumchloride.
 Wat is de chemische formule voor koolstof en zuurstof?
Wat is de chemische formule voor koolstof en zuurstof?  Het aantal mol opgeloste stof bepalen
Het aantal mol opgeloste stof bepalen  Is een atoom met 12 protonen elektronen en neutronen-ionen?
Is een atoom met 12 protonen elektronen en neutronen-ionen?  Hoe kunnen we zout-alkalibodems effectief verbeteren en gebruiken om de voedselzekerheid te garanderen?
Hoe kunnen we zout-alkalibodems effectief verbeteren en gebruiken om de voedselzekerheid te garanderen?  Aantal elektronen aanwezig in een neutraal bariumatoom?
Aantal elektronen aanwezig in een neutraal bariumatoom?
 Een positieve kant aan die verschrikkelijke rapporten over klimaatverandering?
Een positieve kant aan die verschrikkelijke rapporten over klimaatverandering? Studie kan strategieën verbeteren om de afvoer van nutriënten naar de Mississippi te verminderen
Studie kan strategieën verbeteren om de afvoer van nutriënten naar de Mississippi te verminderen De effecten van stortplaatsen op het milieu
De effecten van stortplaatsen op het milieu Microbeads in cosmetica zijn misschien al onderweg, nieuw onderzoek suggereert:
Microbeads in cosmetica zijn misschien al onderweg, nieuw onderzoek suggereert: Radar voegt een technologische draai toe aan het eeuwenoude telproces van cranberry's
Radar voegt een technologische draai toe aan het eeuwenoude telproces van cranberry's
Hoofdlijnen
- Waarom komt DNA -synthese op?
- Wanneer citroenen je leven geven:Herpetofauna-aanpassing aan citrusboomgaarden in Belize
- Wat eten diep watervissen?
- Wat is de Bactrische niche?
- Wat is anaëroob?
- Waar bestaan P en L uit?
- Wat is het wetenschappelijke proces?
- Waarom wetenschappers een ondergronds mysterie willen oplossen over waar microben leven
- Waar in het lichaam gebeurt ademhaling?
- De universele taal van hormonen

- Gefossiliseerde algen zijn veelbelovend voor verbeterde voedselveiligheidstesten
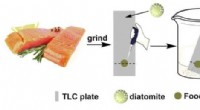
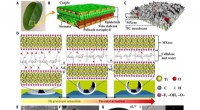
- Bio-geïnspireerde op MXene gebaseerde actuatoren voor programmeerbare slimme apparaten
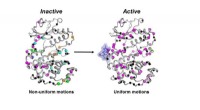
- Enzymenbeweging kan de sleutel zijn tot nieuwe kankermedicijnen
- Nieuwe trucjes leren van zeesponzen, naturen meest onwaarschijnlijke civiel ingenieurs

 Nieuwe methode maakt weersvoorspellingen zo goed als regen
Nieuwe methode maakt weersvoorspellingen zo goed als regen Honden en zwerfdieren lijden onder de hittegolf in Azië
Honden en zwerfdieren lijden onder de hittegolf in Azië  Waarom is benzoëzuur beter oplosbaar in een alkalische oplossing dan in een neutrale oplossing?
Waarom is benzoëzuur beter oplosbaar in een alkalische oplossing dan in een neutrale oplossing?  Wat is de formule voor ammoniumion?
Wat is de formule voor ammoniumion?  Waar zijn de ionisatie nevels voornamelijk gelegen?
Waar zijn de ionisatie nevels voornamelijk gelegen?  Wanneer een chromosoom op zichzelf in karyotype verschijnt en niet als paar staat het bekend als?
Wanneer een chromosoom op zichzelf in karyotype verschijnt en niet als paar staat het bekend als?  Wat zijn 3 voorbeelden van energietransformaties voor een brandende kaars?
Wat zijn 3 voorbeelden van energietransformaties voor een brandende kaars?  Wetenschappers ontdekken hoe dendrietvorming in batterijen kan worden voorkomen
Wetenschappers ontdekken hoe dendrietvorming in batterijen kan worden voorkomen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

