
Wetenschap
Hoe verandert de opstelling van elektronen wanneer natrium reageert met chloor om chloride te vormen?
natrium (na)
* Initiële status: Natrium heeft 1 elektron in zijn buitenste schaal (valentieschaal). Het heeft de elektronische configuratie 2, 8, 1.
* verlangen: Natrium wil dit enkele valentie -elektron verliezen om een stabiel octet (8 elektronen) in zijn buitenste schaal te bereiken, zoals de edelgassen.
chloor (CL)
* Initiële status: Chloor heeft 7 elektronen in zijn buitenste schaal. De elektronische configuratie is 2, 8, 7.
* verlangen: Chloor wil één elektron winnen om zijn octet te voltooien en stabiel te worden.
De reactie:
1. Elektronenoverdracht: Wanneer natrium- en chloor reageren, geeft natrium zijn enkele valentie -elektron op chloor gemakkelijk op.
2. ionenvorming: Natrium, na een elektron te hebben verloren, wordt een positief geladen ion (NA⁺). Chloor, na een elektron te hebben gewonnen, wordt een negatief geladen ion (CL⁻).
3. ionische binding: De tegengesteld geladen ionen worden sterk tot elkaar aangetrokken en vormen een ionische binding. Dit creëert het samengestelde natriumchloride (NaCl).
Laatste status:
* natrium (Na⁺): Heeft nu de elektronische configuratie 2, 8. Het heeft een compleet octet en een positieve lading.
* chloor (Cl⁻): Heeft nu de elektronische configuratie 2, 8, 8. Het heeft een compleet octet en een negatieve lading.
Sleutelpunten:
* De reactie wordt aangedreven door het verlangen van beide atomen om een stabiele octetconfiguratie te bereiken.
* Deze elektronenoverdracht resulteert in de vorming van ionen met tegengestelde ladingen.
* De sterke elektrostatische aantrekkingskracht tussen deze ionen creëert de ionische binding en houdt de natriumchloride samen.
 Historische klimaatgegevens in de Oost-Aziatische regio redden
Historische klimaatgegevens in de Oost-Aziatische regio redden Klimaatwetenschappers maken Caribische droogteatlas
Klimaatwetenschappers maken Caribische droogteatlas China's afvalverbod zet Amerikaanse recycling op z'n kop - is het tijd om verbranding te heroverwegen?
China's afvalverbod zet Amerikaanse recycling op z'n kop - is het tijd om verbranding te heroverwegen? Hoe schimmels kunnen bijdragen aan een groene bouwsector
Hoe schimmels kunnen bijdragen aan een groene bouwsector Waarom fotosyniseren planten in een veld 's nachts slechts?
Waarom fotosyniseren planten in een veld 's nachts slechts?
Hoofdlijnen
- Vogels versus bijen:studie helpt verklaren hoe bloemen evolueerden om bestuivers te specialiseren
- Voorbereiden op toekomstige coronavirusvarianten met behulp van kunstmatige intelligentie
- Zijn de antibiotica lipiden in de natuur?
- Welke elementen zijn de belangrijkste contituenten van het levende organisme?
- Wat is de medische term die niet betekent dat niet -ranselcel niet is?
- Waarom is het menselijk ras zo dirkerend?
- Wat wordt gebruikt om te zien of twee organismen gerelateerd zijn?
- Kunnen nijlpaarden vleeseters zijn?
- Welke structuur ontwikkelt zich tot het ruggenmerg van gewervelde dieren?
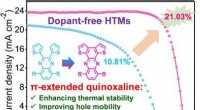
- Doteringsvrij, vochtstabiele organische lagen geven perovskiet-zonnecellen 21% efficiëntie
- Hoe plankton en bacteriën oceaanspray vormen

- Hoe maak je het gemakkelijker om plantaardig afval om te zetten in biobrandstoffen?

- Klein worden om te bepalen waar nucleair materiaal vandaan komt en hoe het is gemaakt

- Handgebreide moleculen

 Wat is de regenschaduw van een berg?
Wat is de regenschaduw van een berg?  Science Fair-projecten op handversmettingsmiddelen of vloeibare zeep voor het doden van bacteriën
Science Fair-projecten op handversmettingsmiddelen of vloeibare zeep voor het doden van bacteriën Wat is een reactant die bindt aan katalysator?
Wat is een reactant die bindt aan katalysator?  Op welke temperatuur verbrandt ammoniak?
Op welke temperatuur verbrandt ammoniak?  Methoden voor machinaal leren leiden tot ontdekking van zeldzame quasars met viervoudige afbeelding
Methoden voor machinaal leren leiden tot ontdekking van zeldzame quasars met viervoudige afbeelding In de reactie MGCI2 plus 2KOH MGOH2 2KCI Hoeveel mol worden er geproduceerd voor elke mol mgcl2?
In de reactie MGCI2 plus 2KOH MGOH2 2KCI Hoeveel mol worden er geproduceerd voor elke mol mgcl2?  Minimalisering van de uitstoot van ammoniakbrandstof
Minimalisering van de uitstoot van ammoniakbrandstof Een webcam is voldoende om een realtime 3D-model van een bewegende hand te maken
Een webcam is voldoende om een realtime 3D-model van een bewegende hand te maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

