
Wetenschap
Monster van mengsel dat kan worden gescheiden door destillatie?
monster van een mengsel dat kan worden gescheiden door destillatie:
zoutwater
Verklaring:
* zoutwater is een homogeen mengsel van zout (NaCl) opgelost in water (H₂o).
* destillatie vertrouwt op het verschil in kookpunten tussen de componenten van een mengsel.
* Water heeft een aanzienlijk lager kookpunt (100 ° C) dan zout (die pas 801 ° C smelt).
* Wanneer verwarmd, het water zal verdampen en in stoom veranderen, waardoor het zout blijft achter.
* De stoom wordt vervolgens terug in vloeibaar water, resulterend in de scheiding van de twee componenten.
Andere voorbeelden:
* ethanol en water: Ethanol heeft een lager kookpunt dan water.
* Ruwe olie: Distillatie wordt gebruikt om ruwe olie in verschillende fracties te scheiden op basis van hun kookpunten, zoals benzine, kerosine en diesel.
* azijn: Azijn is een mengsel van azijnzuur en water. Azijnzuur heeft een lager kookpunt dan water.
Opmerking: Distillatie is effectief voor het scheiden van mengsels waarbij de componenten aanzienlijk verschillende kookpunten hebben. Het is niet geschikt voor mengsels met componenten met vergelijkbare kookpunten.
 Behoud van trillingscoherentie met elektronenspin
Behoud van trillingscoherentie met elektronenspin Wordt calciumbicarbonaat gevormd wanneer carbone dioxide en water chemisch combineren?
Wordt calciumbicarbonaat gevormd wanneer carbone dioxide en water chemisch combineren?  Is zinkfosfide een metallisch zout?
Is zinkfosfide een metallisch zout?  Corbin komt vóór stikstof op het periodiek systeem vanwege koolstof?
Corbin komt vóór stikstof op het periodiek systeem vanwege koolstof?  Wetenschappers ontdekken fijne kneepjes van serotoninereceptor die cruciaal zijn voor betere therapieën
Wetenschappers ontdekken fijne kneepjes van serotoninereceptor die cruciaal zijn voor betere therapieën
 Verbrande bomen en miljarden in contanten:hoe een klimaatprogramma in Californië ervoor zorgt dat bedrijven blijven vervuilen
Verbrande bomen en miljarden in contanten:hoe een klimaatprogramma in Californië ervoor zorgt dat bedrijven blijven vervuilen Aardbevingen in Raton Basin gekoppeld aan injecties van olie en gasvloeistof
Aardbevingen in Raton Basin gekoppeld aan injecties van olie en gasvloeistof NASA vindt windschering die tropische depressie Erin . beïnvloedt
NASA vindt windschering die tropische depressie Erin . beïnvloedt Hoeveel zintuigen heeft de mens?
Hoeveel zintuigen heeft de mens?  Welke soorten vissen eten Eendekroos?
Welke soorten vissen eten Eendekroos?
Hoofdlijnen
- Genomische analyse van een soort zoöplankton stelt aannames over soortvorming en genregulatie in vraag
- Onderzoekers genereren tomaten met verbeterde antioxiderende eigenschappen door genetische manipulatie
- Cellen gestrest? Maak de mitochondriën langer
- Gebruikt cellulaire ademhaling NADPH als zijn elektronendrager?
- Hoe een klein en vreemd zeedier gedurende zijn hele leven onbeperkt sperma produceert
- Elektronenmicroscoopbeelden laten zien hoe cellen een vitaal mineraal opnemen
- Gewelddadige dromen kunnen een aanwijzing zijn waarom dromen zijn geëvolueerd, zeggen onderzoekers
- Reacties van zaadeigenschappen op extreme droogte impliceren sterke relaties met droogtegevoeligheid
- Welke besmettelijke ziekte valt de witte bloedcellen aan?
- Studie onthult mogelijk nieuw behandeldoel in de strijd tegen COVID-19
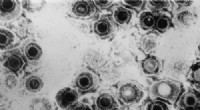
- Cryo-elektronenmicroscopie onthult gemeenschappelijke herpesvirusstructuur
- Sterk en kneedbaar Damascus-staal door additieve fabricage

- Lab-on-a-chip rijdt op zoek naar nieuwe medicijnen om bloedstolsels te voorkomen

- Een eerste in zijn soort katalysator bootst natuurlijke processen na om plastic af te breken en waardevolle nieuwe producten te produceren

 NASA-bodemvochtgegevens bevorderen wereldwijde gewasprognoses
NASA-bodemvochtgegevens bevorderen wereldwijde gewasprognoses Waar is de massa van een atoom gecentreerd?
Waar is de massa van een atoom gecentreerd?  Hoe produceert de zon energie?
Hoe produceert de zon energie?  Onderzoekers voeren eerste natuurkundige basissimulatie uit van de impact van gerecyclede atomen op plasmaturbulentie
Onderzoekers voeren eerste natuurkundige basissimulatie uit van de impact van gerecyclede atomen op plasmaturbulentie Verbetering van kleefstoffen voor draagbare sensoren
Verbetering van kleefstoffen voor draagbare sensoren Wat gebruikte Thomas Edison in filamenten?
Wat gebruikte Thomas Edison in filamenten?  Hoop om zeker tekenen van leven op Mars te ontdekken? Nieuw onderzoek zegt zoek naar het element vanadium
Hoop om zeker tekenen van leven op Mars te ontdekken? Nieuw onderzoek zegt zoek naar het element vanadium Welke chemische veranderingen vinden plaats in de hersenen als je lacht?
Welke chemische veranderingen vinden plaats in de hersenen als je lacht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

