
Wetenschap
Hoeveel subatomaire deeltjes in chloor?
Inzicht in subatomaire deeltjes
* protonen: Positief geladen deeltjes gevonden in de kern van een atoom. Het aantal protonen definieert het element.
* neutronen: Neutraal geladen deeltjes gevonden in de kern van een atoom. Het aantal neutronen kan variëren binnen een element, wat leidt tot isotopen.
* elektronen: Negatief geladen deeltjes die de kern in elektronenschalen draaien. Het aantal elektronen is meestal gelijk aan het aantal protonen om neutraliteit te behouden.
chloor (CL)
* Atomisch nummer: 17. Dit betekent dat chloor 17 protonen heeft.
* Atomische massa: Ongeveer 35,45. Dit is een gemiddelde van de massa van alle chloorisotopen.
Subatomaire deeltjes berekenen
* protonen: 17 (gedefinieerd door het atoomnummer)
* elektronen: 17 (gelijk aan het aantal protonen in een neutraal atoom)
* neutronen: Dit is een beetje lastiger. U moet de meest voorkomende isotoop van chloor vinden. Chloor -35 is de meest voorkomende, wat betekent dat het 18 neutronen heeft (35 - 17 =18).
Belangrijke opmerking: Het aantal neutronen kan variëren, wat leidt tot verschillende chloorisotopen. Chloor -37 is een andere isotoop met 20 neutronen (37 - 17 =20).
Samenvatting
* protonen: 17
* elektronen: 17
* neutronen: Meest voorkomende isotoop (chloor-35):18
 Een stroomdiagram voor biologie maken
Een stroomdiagram voor biologie maken Wanneer een opgeloste stof in water oplost, wat doet het vriespunt?
Wanneer een opgeloste stof in water oplost, wat doet het vriespunt?  Hoe is chemie gerelateerd aan een ander wetenschapsgebied?
Hoe is chemie gerelateerd aan een ander wetenschapsgebied?  Knijp de schok eruit:wat verschillende fasen van piëzo-elektrische materialen ons vertellen?
Knijp de schok eruit:wat verschillende fasen van piëzo-elektrische materialen ons vertellen? Cheminformatics-benaderingen voor het maken van nieuwe haarkleurmiddelen
Cheminformatics-benaderingen voor het maken van nieuwe haarkleurmiddelen
 Wat de dood van een eenzame inheemse man in Brazilië ons kan vertellen over onze wereldwijde toekomst
Wat de dood van een eenzame inheemse man in Brazilië ons kan vertellen over onze wereldwijde toekomst Wat zit er achter de terugtrekkende kelpen en uitzettende koralen?
Wat zit er achter de terugtrekkende kelpen en uitzettende koralen? Wetenschappers stellen een nieuwe methode voor om de ongrijpbare oorsprong van CO₂-uitstoot uit stromen te volgen
Wetenschappers stellen een nieuwe methode voor om de ongrijpbare oorsprong van CO₂-uitstoot uit stromen te volgen  Arctische stoofpot:begrijpen hoe meren op hoge breedtegraden reageren op en invloed hebben op de klimaatverandering
Arctische stoofpot:begrijpen hoe meren op hoge breedtegraden reageren op en invloed hebben op de klimaatverandering  Nieuw onderzoek ontsluit het mysterie van de stranden van New England
Nieuw onderzoek ontsluit het mysterie van de stranden van New England
Hoofdlijnen
- Wat beschrijft nauwkeurig hoe temperatuur de enzymactiviteit beïnvloedt?
- Wetenschappers identificeren hoe de ontwikkeling van verschillende soorten dezelfde genen met verschillende kenmerken gebruikt
- Witte wijn van Grüner Veltliner zou de toast van Pennsylvania kunnen zijn, suggereert onderzoek
- De straf van het hebben van een zus - waarom seks tussen broers en zussen belangrijk is voor mannelijke saiga-antilopen
- Hoe diversifiëren en fylogenetisch correleren functionele kenmerken voor gelijktijdig voorkomende ondersoorten in boreale bossen?
- Welke 2 delen van een plantencel bieden structuur?
- Uit welk deel van de hersenen komt cognitie?
- Wat is de rol van ATP in celdeling?
- Wat is de evolutietheorie door natuurlijke selectie?
- Lichtgevoelig molecuul helpt zeedieren hun voortplantingscyclus te synchroniseren
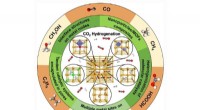
- Beoordeling van technologieën die het potentieel voor de omzetting van kooldioxide in bruikbare producten vergroten
- Hoe chemische reacties worden berekend

- De rol van hydrofobe moleculen in katalytische reacties

- Biokatalyse:nieuwe methode om katalytisch actieve enzymen aan te drijven

 Wat is het nekbot van de wetenschappelijke naam?
Wat is het nekbot van de wetenschappelijke naam?  Publiceren senior docenten net zoveel als hun jongere collega's?
Publiceren senior docenten net zoveel als hun jongere collega's? Welke verklaring probeert in de wetenschappelijke methode een waargenomen fenomeen te verklaren?
Welke verklaring probeert in de wetenschappelijke methode een waargenomen fenomeen te verklaren?  Crowdfunding uit de pandemie komt vaker voor, succesvol in welvarende gemeenschappen
Crowdfunding uit de pandemie komt vaker voor, succesvol in welvarende gemeenschappen Wat is een plant die bestaat uit zowel schimmels als algen?
Wat is een plant die bestaat uit zowel schimmels als algen?  Online trollen was vroeger grappig, maar nu verwijst de term naar iets veel sinisters
Online trollen was vroeger grappig, maar nu verwijst de term naar iets veel sinisters Dieren die vlees en planten eten
Dieren die vlees en planten eten  Wat is de biologische functie van zwavel?
Wat is de biologische functie van zwavel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

