
Wetenschap
Wat voor soort diagrammen zijn natriumzuurstof en neon?
1. Lewis dot -diagrammen:
* Doel: Toon de valentie -elektronen (elektronen in de buitenste schaal) van een atoom.
* Hoe ze werken:
* Natrium (NA):heeft 1 valentie -elektron, dus het wordt weergegeven als NA met één stip.
* Oxygen (O):heeft 6 valentie -elektronen, dus het wordt weergegeven als O met zes stippen (twee paren en twee enkele stippen).
* Neon (NE):heeft 8 valentie -elektronen (een volledige buitenste schaal), dus het wordt weergegeven als NE met acht punten.
2. Bohr -modellen:
* Doel: Toon de opstelling van elektronen in schelpen rond de kern.
* Hoe ze werken:
* Teken een kern (bevattende protonen en neutronen) in het midden.
* Teken cirkels rond de kern om energieniveaus (schalen) weer te geven.
* Vul de schalen met stippen die elektronen vertegenwoordigen, volgens de regels van hoeveel elektronen elke schaal kunnen vasthouden.
Voorbeeld:
* natrium (NA): 11 protonen, 11 elektronen.
* De eerste schaal bevat 2 elektronen.
* De tweede schaal bevat 8 elektronen.
* De derde schaal bevat 1 elektron.
* zuurstof (O): 8 protonen, 8 elektronen.
* De eerste schaal bevat 2 elektronen.
* De tweede schaal bevat 6 elektronen.
* neon (ne): 10 protonen, 10 elektronen.
* De eerste schaal bevat 2 elektronen.
* De tweede schaal bevat 8 elektronen (vol).
3. Elektronenconfiguratiediagrammen:
* Doel: Toon de verdeling van elektronen in specifieke energieniveaus (orbitalen) in het atoom.
* Hoe ze werken:
* Gebruik een notatiesysteem zoals 1S², 2S², 2P⁶, enz. Om de orbitalen en hun elektronenbezetting weer te geven.
Voorbeeld:
* natrium (NA): 1S² 2S² 2P⁶ 3S¹
* zuurstof (O): 1S² 2S² 2P⁴
* neon (ne): 1S² 2S² 2P⁶
4. Andere diagrammen:
* orbitale diagrammen: Toon de vormen en oriëntaties van atomaire orbitalen in 3D -ruimte.
* Moleculaire orbitale diagrammen: Beschrijf binding in moleculen door de combinatie van atomaire orbitalen te tonen.
Belangrijke opmerking: Het specifieke diagram dat u gebruikt, is afhankelijk van de context en wat u wilt illustreren. Lewis DOT -diagrammen zijn goed voor het snel tonen van valentie -elektronen, terwijl Bohr -modellen een visuele weergave van elektronenschalen geven. Elektronenconfiguratiediagrammen zijn meer gedetailleerd en nuttig voor het begrijpen van chemische binding en reactiviteit.
Hoofdlijnen
- Hebben wangcellen membraangebonden organellen?
- Verdediging tegen bijna elke prijs
- IJzer-zwavelmineralen kunnen getuigen van de eerste microben op aarde die miljarden jaren geleden leefden
- Hoe worden ze gegroepeerd in de kern?
- Onderzoeken hoe bryofyten zich aanpassen zonder gibberelline
- Hoe meet je geluk?
- Hoe je een groter brein kunt laten groeien
- Plaats van secretoire en membraaneiwitsynthese?
- Uit onderzoek blijkt dat Australische grotten tot 500.000 jaar ouder zijn dan we dachten, en het zou een megafauna-mysterie kunnen verklaren
- Ontdekking verhoogt de mogelijkheid om neurologische aandoeningen te behandelen

- Thuis COVID-19-tests:hoe goed zijn ze?
- Een keramische aerogel gemaakt met nanokristallen en ingebed in een matrix voor gebruik in thermische isolatietoepassingen

- Machine-learningsysteem versnelt ontdekking van nieuwe materialen voor 3D-printen

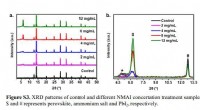
- Efficiënte perovskiet-zonnecellen ontwikkeld door interface-gemedieerde recombinatie te verminderen
 Hoe kun je de massa van de aarde berekenen?
Hoe kun je de massa van de aarde berekenen?  Hoe biobrandstoffen uit plantaardige vezels de opwarming van de aarde kunnen tegengaan
Hoe biobrandstoffen uit plantaardige vezels de opwarming van de aarde kunnen tegengaan  Rijd met Juno terwijl hij langs de grootste maan van het zonnestelsel en Jupiter vliegt
Rijd met Juno terwijl hij langs de grootste maan van het zonnestelsel en Jupiter vliegt Verschil tussen een regulator en een conformer
Verschil tussen een regulator en een conformer  IJslandse vulkaanuitbarsting langste in halve eeuw
IJslandse vulkaanuitbarsting langste in halve eeuw Exotisch elektronisch effect gevonden in 2D-topologisch materiaal
Exotisch elektronisch effect gevonden in 2D-topologisch materiaal Een eenvoudige methode om vlakke microstructuren van polysiloxaan af te drukken
Een eenvoudige methode om vlakke microstructuren van polysiloxaan af te drukken In wat voor soort energie dat laat het licht omzetten?
In wat voor soort energie dat laat het licht omzetten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


