
Wetenschap
Wat is de oxidatie halve reactie van CL2 2CU tot 2CUCl?
Hier leest u hoe u de oxidatiehalfreactie kunt afbreken:
1. Identificeer de oxidatie
* koper (cu) wordt geoxideerd omdat het van een elementaire toestand (0 oxidatietoestand) naar een +1 oxidatietoestand in CUCL gaat.
2. Schrijf de halfreactie
De oxidatie halfreactie richt zich alleen op het koper:
Cu (s) → cu⁺ (aq) + e⁻
Verklaring
* cu (s): Solide koperatomen verliezen een elektron.
* cu⁺ (aq): Koperionen in oplossing (waterig).
* E⁻: Het verloren elektron.
Belangrijke opmerking: Het chloor (CL₂) wordt in deze reactie verminderd en u zou een afzonderlijke reductiehalfreactie moeten schrijven om het totale proces volledig weer te geven.
 Is honing een mengsel of samengesteld?
Is honing een mengsel of samengesteld?  Apparaat verfijnt analyse van materialen voor brandstofcellen en batterijen
Apparaat verfijnt analyse van materialen voor brandstofcellen en batterijen Chemici synthetiseren unieke antikankermoleculen met behulp van een nieuwe aanpak
Chemici synthetiseren unieke antikankermoleculen met behulp van een nieuwe aanpak  Welke elementen maken natuurlijke diamanten?
Welke elementen maken natuurlijke diamanten?  Wat gebeurt er als zoutzuur en natriumethanoaat worden gecombineerd?
Wat gebeurt er als zoutzuur en natriumethanoaat worden gecombineerd?
Hoofdlijnen
- Een genetische trigger voor de Cambrische explosie ontrafeld?
- Welke orgel slaat een mix van afval en water op totdat het klaar is om het lichaam te verlaten?
- Nieuwe cijfers laten een bevolkingsgroei zien in de buurt van de kwetsbare koraalriffen ter wereld
- Wat zijn de vier fabrieksprocessen?
- Welke studie helpt je om de redenering van de redenering te begrijpen?
- Wat zou een sociaal -wetenschapper waarschijnlijk studeren?
- Stadia van meiose met een beschrijving
- Is gelelektroforese een belangrijk hulpmiddel dat in de biotechnologie wordt gebruikt voor forensisch onderzoek en vaderschapstests?
- Reageren alle delen van de plant op dezelfde manier op stimuli?
- Het probleem oplossen:organische damp veroorzaakt het oplossen van moleculaire zouten

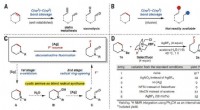
- Zilverzout dat wordt gebruikt om C-C-bindingen in ongespannen cyclische aminen te verbreken
- St. Janskruid bloemen dienen als groene katalysator

- Onderzoekers rapporteren nieuwe methode voor het karakteriseren van materialen die uiteindelijk kunnen helpen energie op te slaan

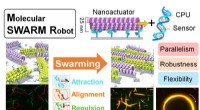
- Wetenschappers werken eraan om robots ter grootte van een molecuul samen te laten zwermen om taken uit te voeren
 Is chemische formule h20 een fysieke of eigenschap?
Is chemische formule h20 een fysieke of eigenschap?  Auxine zorgt voor bladafvlakking
Auxine zorgt voor bladafvlakking Het totale aantal verduistering elk jaar is niet hoger dan?
Het totale aantal verduistering elk jaar is niet hoger dan?  Nieuw nanodeeltje stopt multiple sclerose, wordt nu getest bij diabetes type 1 en astma
Nieuw nanodeeltje stopt multiple sclerose, wordt nu getest bij diabetes type 1 en astma Wat zijn elk jaar twee dagen wanneer de zon precies opkomt vanwege het oosten en naar het westen gaat?
Wat zijn elk jaar twee dagen wanneer de zon precies opkomt vanwege het oosten en naar het westen gaat?  Hoe NASA's Romeinse telescoop de leeftijd van sterren zal meten
Hoe NASA's Romeinse telescoop de leeftijd van sterren zal meten  Walvisontmoetingen in Mexico benadrukken de noodzaak van wereldwijde investeringen in onderzoek naar bultruggen
Walvisontmoetingen in Mexico benadrukken de noodzaak van wereldwijde investeringen in onderzoek naar bultruggen  Verticale pensioneringsdorpen zijn in opkomst, en ze zijn ook hightech
Verticale pensioneringsdorpen zijn in opkomst, en ze zijn ook hightech
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

