
Wetenschap
Wat is fluorreactie met aluminium?
Reactievergelijking:
2 AL (s) + 3 f 2 (g) → 2 ALF 3 (S)
Reactiebeschrijving:
* Initiatie: Fluor is een zeer reactief niet -metaal en de reactie ervan met aluminium is spontaan bij kamertemperatuur.
* verbranding: De reactie genereert een heldere, witte vlam terwijl het aluminium brandt in het fluorgas.
* Vorming van aluminium fluoride: Aluminium fluoride is een witte, vaste verbinding die wordt gevormd als gevolg van de reactie.
* Warmte en licht: De reactie geeft significante warmte- en lichte energie vrij, waardoor het zeer exotherme is.
Veiligheidsmaatregelen:
Fluor is een zeer corrosief en giftig gas. Het is extreem gevaarlijk om te hanteren en de reactie ervan met aluminium is zeer gevaarlijk. Probeer nooit deze reactie uit te voeren zonder de juiste veiligheidsuitrusting en training.
Gebruik van aluminium fluoride:
Aluminium fluoride is een belangrijke industriële chemische stof die wordt gebruikt in:
* productie van aluminium: Het wordt gebruikt als een flux in de elektrolytische productie van aluminium.
* Glasproductie: Het wordt gebruikt bij de productie van glas en keramiek.
* Andere toepassingen: Het wordt ook gebruikt als een katalysator, een pesticide en een houtconserveermiddel.
 Hoe maken ratten nesten?
Hoe maken ratten nesten?  Braziliaanse officier van justitie beveelt aan om Total-olievergunning in de buurt van Amazon te weigeren
Braziliaanse officier van justitie beveelt aan om Total-olievergunning in de buurt van Amazon te weigeren Dit is het moment om vragen te beantwoorden over de gevolgen van klimaatverandering voor ziekten
Dit is het moment om vragen te beantwoorden over de gevolgen van klimaatverandering voor ziekten Waarom je bijna zeker tijd verspilt aan het spoelen van je recycling?
Waarom je bijna zeker tijd verspilt aan het spoelen van je recycling? Groot opslagpotentieel in toekomstige ijsvrije gletsjerbassins
Groot opslagpotentieel in toekomstige ijsvrije gletsjerbassins
Hoofdlijnen
- Bijen vertonen geavanceerde leervaardigheden
- Historische tekens in het landschap:onderzoek naar de praktijk van knotten in West-Noorwegen
- Jura-dinosaurus met vogelschild was een van de eersten die in kuddes leefde
- Twee vormen van c6h1206 die eenvoudige suikers zijn:glucose en?
- Wat is de functie van mitochondriën in eukayotische organismen?
- Wat is Proteanics?
- Is de computer een goed model voor de hersenen?
- Hoe de egoïstische genen van gist slagen
- Welke celstructuur is gemeenschappelijk voor alle cellen?
- Kleine kooien kunnen vaccins veilig houden bij hoge temperaturen
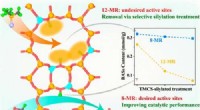
- Nieuwe strategie om de verspreiding van zuurplaatsen in zeolieten te beheersen
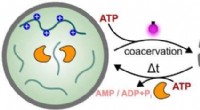
- Hoe licht kan worden gebruikt om processen in synthetische cellen te controleren
- Het produceren van ammoniak via elektrochemische processen kan de uitstoot van kooldioxide verminderen

- Nieuwe methode meet 3D-polymeerverwerking nauwkeurig
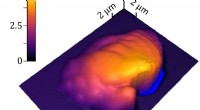
 Uitbreidingsmicroscopie en virtual reality verlichten nieuwe manieren om ziekten te voorkomen en te behandelen
Uitbreidingsmicroscopie en virtual reality verlichten nieuwe manieren om ziekten te voorkomen en te behandelen NASA vangt tropische cycloon Gelenas post-tropische overgang
NASA vangt tropische cycloon Gelenas post-tropische overgang Nieuw rekenmodel maakt nucleaire magnetische resonantie een nog krachtiger hulpmiddel voor onderzoekers
Nieuw rekenmodel maakt nucleaire magnetische resonantie een nog krachtiger hulpmiddel voor onderzoekers Hoe kan iemand weten dat het punt van licht een satelliet is in een lage baan en geen ster is?
Hoe kan iemand weten dat het punt van licht een satelliet is in een lage baan en geen ster is?  Welke maand was de Orion het meest zichtbaar?
Welke maand was de Orion het meest zichtbaar?  Hoeveel elektronen zal kalium winnen of verliezen bij het vormen van een ion?
Hoeveel elektronen zal kalium winnen of verliezen bij het vormen van een ion?  Veranderingen in de grootte van de rat onthullen de habitat van de Hobbit-hominine
Veranderingen in de grootte van de rat onthullen de habitat van de Hobbit-hominine Wetenschap doen, in plaats van wetenschappers te zijn, meer bemoedigend voor degenen die ondervertegenwoordigd zijn in het veld
Wetenschap doen, in plaats van wetenschappers te zijn, meer bemoedigend voor degenen die ondervertegenwoordigd zijn in het veld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

