
Wetenschap
Binaire ionische verbinding waarin het anion en het kation elk 10 elektronen hebben?
Inzicht in het concept
* Binaire ionische verbindingen: Deze verbindingen bestaan uit een metaalkation (positief geladen ion) en een niet -metaalanion (negatief geladen ion).
* 10 elektronen: Atomen met 10 elektronen zijn iso -elektronisch met de Noble Gas Neon (NE). Dit betekent dat ze dezelfde elektronenconfiguratie hebben als neon.
het vinden van de elementen
1. kation: Om 10 elektronen te hebben, moet het kation elektronen hebben verloren. Dit betekent dat het een metaal moet zijn dat oorspronkelijk meer dan 10 elektronen had. Zoek naar elementen in groepen 1, 2 of 3 op het periodieke tabel.
* natrium (NA): Natrium heeft 11 elektronen en verliest er een om Na+ te worden met 10 elektronen.
* magnesium (mg): Magnesium heeft 12 elektronen en verliest twee om Mg2+ te worden met 10 elektronen.
* aluminium (AL): Aluminium heeft 13 elektronen en verliest drie om Al3+ te worden met 10 elektronen.
2. anion: Om 10 elektronen te hebben, moet het anion elektronen hebben gewonnen. Dit betekent dat het een niet -metaal moet zijn die oorspronkelijk minder dan 10 elektronen had. Zoek naar elementen in groepen 16 of 17 op het periodieke tabel.
* zuurstof (O): Zuurstof heeft 8 elektronen en wint twee om O2 te worden met 10 elektronen.
* fluor (f): Fluor heeft 9 elektronen en wint één om F- te worden met 10 elektronen.
Mogelijke verbindingen
Op basis van het bovenstaande kunnen we verschillende mogelijke binaire ionische verbindingen vormen:
* Na2o (Natriumoxide)
* mgo (Magnesiumoxide)
* al2o3 (Aluminiumoxide)
* NAF (Natriumfluoride)
* mgf2 (Magnesiumfluoride)
* alf3 (Aluminium fluoride)
Opmerking: Er kunnen andere mogelijkheden zijn als we minder veel voorkomende ionen beschouwen, maar dit zijn de meest waarschijnlijke scenario's.
 Wetenschappers ontdekken dat de balans tussen thermische energie en lage klimaatstress de diversiteit van koraalsoorten stimuleert
Wetenschappers ontdekken dat de balans tussen thermische energie en lage klimaatstress de diversiteit van koraalsoorten stimuleert Herwild 25% van het VK voor minder klimaatverandering, meer dieren in het wild en een leven dichter bij de natuur
Herwild 25% van het VK voor minder klimaatverandering, meer dieren in het wild en een leven dichter bij de natuur Sri Lanka keert biologische landbouw terug terwijl thee lijdt
Sri Lanka keert biologische landbouw terug terwijl thee lijdt Een warmere wereld kan meer lokale, minder globaal, temperatuurvariabiliteit
Een warmere wereld kan meer lokale, minder globaal, temperatuurvariabiliteit Was het leven op de vroege aarde paars?
Was het leven op de vroege aarde paars?
Hoofdlijnen
- Welk type bindingen houdt DNA-strengen bij elkaar?
- Genen bieden hoop voor het voortbestaan van Arabië's laatste grote kat
- Hoe interactie met vrouwtjes de agressie bij mannelijke fruitvliegjes verhoogt
- Tot welke functionele groepspolysachariden zijn?
- Oude scheikunde kan verklaren waarom levende wezens ATP gebruiken als de universele energievaluta
- Waarom is het gemakkelijker om de chemische structuur van dode weefsels te bepalen dan levend vlees?
- Kopiëren of innoveren? Studie werpt licht op de chimpanseecultuur
- Wat wordt bedoeld met de stelling dat DNA alle organismen verenigt?
- Waarom leven sommige planten snel en sterven ze jong?
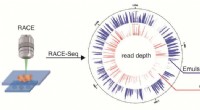
- Onderzoekers verbeteren de methode die het genoom koppelt aan functie voor eencellige omgevingscellen
- Synthetisch gelatineachtig materiaal bootst de rek en sterkte van de onderbuik van kreeft na
- Fusion-wetenschappers hebben een sculptuurtechniek op nanoschaal ontwikkeld
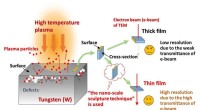
- Emissievrije dieselverbranding met een niet-evenwichtsplasma-ondersteund MnO2-filter

- Natures sweets:een natuurlijk recept lenen voor suikersynthese

 Leonardo da Vinci's nemen dynamisch vliegen over
Leonardo da Vinci's nemen dynamisch vliegen over Nieuwe manieren verkennen om thermische straling te beheersen
Nieuwe manieren verkennen om thermische straling te beheersen Wetenschappers strijken de fysica van rimpels glad
Wetenschappers strijken de fysica van rimpels glad Het uitsluiten van immigranten zonder papieren van stimuleringsfondsen kostte $ 10 miljard aan economische activiteit
Het uitsluiten van immigranten zonder papieren van stimuleringsfondsen kostte $ 10 miljard aan economische activiteit Waarom wordt thermocol gebruikt voor het koelen?
Waarom wordt thermocol gebruikt voor het koelen?  Een nieuwe draai aan de oorsprong van het leven?
Een nieuwe draai aan de oorsprong van het leven?  Hoe kunt u nucleaire explosieven gebruiken in een wetenschapsproject?
Hoe kunt u nucleaire explosieven gebruiken in een wetenschapsproject?  Biologen werpen licht op hoe cellen hulpbronnen verplaatsen
Biologen werpen licht op hoe cellen hulpbronnen verplaatsen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

