
Wetenschap
Balans koper 2 sulfaat pentahydraat wordt verwarmd om de waterhydratatie van de water af te stimuleren?
1. Schrijf de onevenwichtige vergelijking:
CUSO₄ · 5H₂O (S) → CUSO₄ (S) + H₂O (G)
2. Breng de waterstofatomen in evenwicht:
CUSO₄ · 5H₂O (S) → CUSO₄ (S) + 5 H₂o (g)
3. De vergelijking is nu in evenwicht.
Balanced vergelijking:
CUSO₄ · 5H₂O (S) → CUSO₄ (S) + 5H₂O (G)
Verklaring:
* cuso₄ · 5h₂o (s): Koper (II) Sulfaat Pentahydraat, een blauwe vaste stof.
* cuso₄ (s): Watervrij koper (II) sulfaat, een witte vaste stof.
* h₂o (g): Waterdamp.
Sleutelpunten:
* Het proces van het verwarmen van koper (II) sulfaat pentahydraat om de watermoleculen te verwijderen wordt uitdroging genoemd.
* De watermoleculen worden afgedreven als damp.
* Het watervrije koper (II) sulfaat is een witte vaste stof, terwijl het pentahydraat blauw is. Deze kleurverandering is een visuele indicator van het uitdrogingsproces.
Hoofdlijnen
- Wat maakt een verhaal succesvol? Onderzoekers hebben een manier gevonden om dit te voorspellen
- Wat vindt alleen plaats in het reproductieve weefsel van een organisme en tijdens het doorloopt een enkele cel twee divisies?
- Conjugatie geeft een eigenschap door van de ene bacterie naar de andere via een kleine DNA-streng die plasmide wordt genoemd. Waar of niet waar?
- Californië verbiedt de zalmvisserij voor het seizoen in de rivieren in het Sacramento-gebied en het Klamath-bekken
- Wat was er eerst:de kip of het ei?
- Hoe ervoor te zorgen dat biodiversiteitsgegevens EERLIJK, gekoppeld, open en toekomstbestendig zijn
- Hoe muizen de beste vluchtroute kiezen
- Wat is de rol van enzymen bij biologisch wassen?
- Science Fair-projecten met nagellak
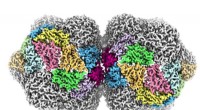
- Verwoestend plantenvirus wordt in atomaire details onthuld
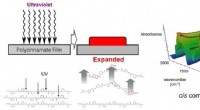
- Fotoexpansie:Biobased polyesters harde film
- Onderzoeker probeert te begrijpen hoe gonorroe resistentie tegen antibiotica ontwikkelt

- Beeldvorming van chemische kinetiek op vloeistof-vloeistof-interfaces
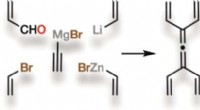
- Gespannen, symmetrisch, en nieuw:tetravinylalleen, een klein maar krachtig molecuul, is voor het eerst gesynthetiseerd
 Biomoleculaire condensaten:onderzoek onthult een slechte voorspellende kracht van gevestigde vloeistof-vloeistoffasescheidingstesten
Biomoleculaire condensaten:onderzoek onthult een slechte voorspellende kracht van gevestigde vloeistof-vloeistoffasescheidingstesten  Onderzoekers openen nieuwe mogelijkheden voor het karakteriseren van interacties tussen nanodeeltjes
Onderzoekers openen nieuwe mogelijkheden voor het karakteriseren van interacties tussen nanodeeltjes Sociologen zorgen ervoor dat water van dichtbij en ver weg stroomt
Sociologen zorgen ervoor dat water van dichtbij en ver weg stroomt Lunar Reconnaissance Orbiter vindt nieuw bewijs van vorst op het oppervlak van de man
Lunar Reconnaissance Orbiter vindt nieuw bewijs van vorst op het oppervlak van de man Oude teksten moedigden hoop en volharding aan toen ze over eindtijd spraken
Oude teksten moedigden hoop en volharding aan toen ze over eindtijd spraken Het gebruik voor galvaniseren
Het gebruik voor galvaniseren Wat gebeurt er als we de zon hebben?
Wat gebeurt er als we de zon hebben?  Nieuwe bacteriesoort ontdekt in de darm
Nieuwe bacteriesoort ontdekt in de darm
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


