
Wetenschap
Waarom zijn sommige metalen betere geleiders dan andere?
1. Aantal gratis elektronen:
* metalen met losjes gebonden valentie -elektronen: Metalen zoals koper, zilver en goud hebben een groot aantal vrije elektronen in hun buitenste schaal (valentieschaal). Deze elektronen zijn gemakkelijk losgemaakt van hun atomen en worden vrij om door de structuur van het metaal te bewegen.
* metalen met strak gebonden valentie -elektronen: Metalen zoals wolfraam, ijzer en nikkel hebben minder vrije elektronen omdat hun valentie -elektronen nauwer zijn gebonden aan hun atomen. Dit beperkt hun geleidbaarheid.
2. Elektronenmobiliteit:
* kristalstructuur: Metalen met een zeer gewone, geordende kristalstructuur, zoals koper, laten elektronen vrij bewegen met minder weerstand.
* onzuiverheden en defecten: De aanwezigheid van onzuiverheden, defecten of korrelgrenzen in de structuur van een metaal kan elektronen verspreiden en de weerstand vergroten.
3. Temperatuur:
* Verhoogde temperatuur, verhoogde weerstand: Naarmate de temperatuur stijgt, trillen atomen meer, waardoor de kans op elektronenverstrooiing vergroot en de geleidbaarheid vermindert.
Voorbeelden:
* zilver is de beste geleider: Het heeft een groot aantal vrije elektronen en een zeer geordende kristalstructuur.
* Koper is een goede tweede: Het is betaalbaarder en op grote schaal gebruikt dan zilver.
* wolfraam heeft een hoge weerstand: Het wordt gebruikt in gloeilampen omdat het hoge temperaturen kan weerstaan zonder te smelten.
Samenvattend:
Metalen met een groot aantal vrije elektronen, een zeer geordende kristalstructuur en minimale onzuiverheden zijn de beste geleiders. Het vermogen van elektronen om vrij te bewegen in het metaal bepaalt de geleidbaarheid ervan. Temperatuur speelt ook een rol, met hogere temperaturen die leiden tot verhoogde weerstand.
 Facebook, Google en Amazon te groot? Waarom die vraag steeds weer opduikt
Facebook, Google en Amazon te groot? Waarom die vraag steeds weer opduikt  De veranderende kleuren van onze levende planeet
De veranderende kleuren van onze levende planeet Nieuwe methode meet zeldzame sporen van een vluchtig gas
Nieuwe methode meet zeldzame sporen van een vluchtig gas Klimaatwetenschappelijk rapport cruciaal voor succes van COP26:UN
Klimaatwetenschappelijk rapport cruciaal voor succes van COP26:UN Nieuwe uitbraak van koraalverbleking in Northern Territory een zorgwekkend teken van onze opwarmende oceanen
Nieuwe uitbraak van koraalverbleking in Northern Territory een zorgwekkend teken van onze opwarmende oceanen
Hoofdlijnen
- Drie verschillen tussen biotische en abiotische componenten van een ecosysteem?
- Vijf nieuwe malariatargets die kunnen leiden tot een effectief vaccin
- Tot ziens 'Zweinstein dinosaurus'? Nieuwe analyses van de groei van dinosauriërs kunnen een derde van de soorten uitroeien
- Wat zijn staafvormige bacteriën?
- 3 geredde dolfijnen zwemmen vrij uit het Indonesische heiligdom
- Wat zijn twee identieke kernen gevormd?
- Wie kreeg de eerste Nobelprijs voor biologie?
- Welk proces produceert genetische diversiteit door willekeurige verdeling van chromosomen?
- Onderzoekers ontsluiten het waterbesparende potentieel van tarwe met TabHLH27 die stress en groei in evenwicht brengt
- Snelle test om een hoge melkkwaliteit te garanderen

- Onderzoek suggereert dat polymeercomposiet kan dienen als lichter, niet-giftige stralingsafscherming

- Een methode bij lage temperaturen voor het maken van hoogwaardige thermo-elektrische materialen

- Onderzoeksteam toont complexe, 3D-geprinte schwarzieten zijn bestand tegen druk wanneer ze zijn gecoat

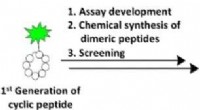
- Screening op macrocyclische peptiden
 Wat is de grootste rivier in het Caribisch gebied?
Wat is de grootste rivier in het Caribisch gebied?  Is nucleïnezuur covalent of ionisch?
Is nucleïnezuur covalent of ionisch?  Zijn er zuivere elementen vloeistoffen bij kamertemperatuur?
Zijn er zuivere elementen vloeistoffen bij kamertemperatuur?  Grafeen:de toekomst in een potloodspoor
Grafeen:de toekomst in een potloodspoor Help, bijen hebben de muren van mijn huis gekoloniseerd! Waarom zijn ze daar en wat moet ik doen?
Help, bijen hebben de muren van mijn huis gekoloniseerd! Waarom zijn ze daar en wat moet ik doen?  Waarom wordt het natriumbenzoaat gemakkelijk geëxtraheerd in H20, terwijl het oorspronkelijke benzoëzuur geen H20 is?
Waarom wordt het natriumbenzoaat gemakkelijk geëxtraheerd in H20, terwijl het oorspronkelijke benzoëzuur geen H20 is?  Hoe snel reizen kometen door de ruimte?
Hoe snel reizen kometen door de ruimte?  Kroatische top oesterkwekers in paniek na gevonden norovirus
Kroatische top oesterkwekers in paniek na gevonden norovirus
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

