
Wetenschap
Wat is Catalyst het gebruik ervan?
Wat is een katalysator?
Een katalysator is een stof die de snelheid van een chemische reactie versnelt zonder in het proces te worden geconsumeerd. Het werkt door een alternatieve reactieroute te bieden met een lagere activeringsenergie , waardoor de reactie sneller zou gaan.
Zie het als een "helper" molecuul dat de reactie vergemakkelijkt zonder zichzelf te veranderen.
Gebruik van katalysatoren:
Katalysatoren zijn essentieel in veel aspecten van ons leven en worden in verschillende industrieën gebruikt. Hier zijn enkele belangrijke voorbeelden:
1. Chemische industrie:
* Productie van kunststoffen, meststoffen en geneesmiddelen: Katalysatoren worden gebruikt om veel essentiële chemicaliën te synthetiseren, waardoor ze efficiënter en milieuvriendelijker worden.
* Raffinage van aardolie: Katalysatoren helpen grote koolwaterstofmoleculen af te breken in kleinere, nuttiger producten zoals benzine en dieselbrandstof.
* Productie van ammoniak: Het Haber-Bosch-proces, dat een katalysator gebruikt om ammoniak te produceren, is cruciaal voor het produceren van meststof en andere stikstofbattende verbindingen.
2. Milieubescherming:
* katalytische converters in auto's: Deze apparaten gebruiken katalysatoren om schadelijke verontreinigende stoffen zoals koolmonoxide, koolwaterstoffen en stikstofoxiden om te zetten in minder schadelijke stoffen zoals koolstofdioxide, water en stikstofgas.
* Afvalwaterzuivering: Katalysatoren kunnen helpen verontreinigende stoffen in afvalwater af te breken, waardoor het veiliger wordt om terug in het milieu te ontladen.
3. Biologische systemen:
* enzymen: Enzymen zijn biologische katalysatoren die essentiële biochemische reacties in levende organismen versnellen, zoals spijsvertering, ademhaling en DNA -replicatie.
4. Energieproductie:
* brandstofcellen: Katalysatoren zijn cruciaal voor het faciliteren van de elektrochemische reacties in brandstofcellen, die chemische energie direct omzetten in elektrische energie.
* hernieuwbare energie: Katalysatoren kunnen worden gebruikt om de efficiëntie van zonnecellen en andere technologieën voor hernieuwbare energie te verbeteren.
Soorten katalysatoren:
* Homogene katalysatoren: Katalysatoren die zich in dezelfde fase (vaste, vloeistof of gas) bevinden als de reactanten.
* heterogene katalysatoren: Katalysatoren die zich in een andere fase bevinden dan de reactanten (bijvoorbeeld vaste katalysator in een vloeistof- of gasreactie).
* biokatalysatoren (enzymen): Katalysatoren afgeleid van biologische bronnen.
Belang van katalysatoren:
* Verhoogde reactiesnelheden: Katalysatoren zorgen ervoor dat reacties sneller doorgaan, waardoor de efficiëntie en de productiviteit toeneemt.
* Verminderd energieverbruik: Katalysatoren verlagen de activeringsenergie, waardoor de behoefte aan hoge temperaturen of druk wordt verminderd.
* Verbeterde selectiviteit: Katalysatoren kunnen de productie van gewenste producten bevorderen, waardoor de vorming van ongewenste bijproducten wordt geminimaliseerd.
* milieuvoordelen: Katalysatoren kunnen vervuiling verminderen en duurzame chemische processen bevorderen.
Katalysatoren zijn een cruciaal onderdeel van veel moderne technologieën en spelen een cruciale rol in een breed scala van industrieën. Hun vermogen om reacties te versnellen en de efficiëntie te verbeteren, heeft hen onmisbare hulpmiddelen gemaakt voor het bevorderen van wetenschap, technologie en ons begrip van de wereld om ons heen.
Hoofdlijnen
- Zombievirussen op een kapingsreis:hoe retrovirale genfragmenten embryonale cellen beïnvloeden
- Cytoskeleton: definitie, structuur en functie (met diagram)
- Hoe kunnen parasieten hun gastheren herkennen?
- Nieuwe inzichten in evolutie:waarom genen lijken te bewegen
- Evolueert de mens sneller? Uit onderzoek blijkt dat we steeds meer verschillend worden, en niet meer hetzelfde
- Welke structuur in de kern bevat erfelijk materiaal?
- Mysterieuze genen overleven de evolutie van mariene organismen
- Bacteriën en blauwgroene algen zijn beide primitief prokaryotisch die op aarde leven?
- Welke eiwitten doen?
- Automatisch en flexibel spaakwielen produceren uit composietmaterialen

- Eiwitstructuur zou nieuwe behandelingen voor cystische fibrose kunnen ontsluiten

- Onderzoekers tonen effectiviteit nieuwe niet-invasieve bloedglucosetest aan
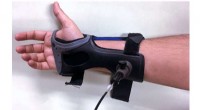
- Nieuw voorgestelde strategie biedt slimme flexibele neurale elektrode met hoge efficiëntie
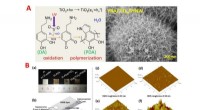
- Enigma van vetzuurmetabolisme opgelost - enzymvorm regelt activiteit
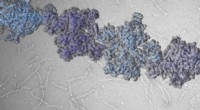
 Hoe worden gletsjervlaktes gevormd?
Hoe worden gletsjervlaktes gevormd?  Luchtvervuiling in verband met gemiste miskramen in China:studie
Luchtvervuiling in verband met gemiste miskramen in China:studie Nieuwe studie onthult de ingrediënten van grote bosbranden
Nieuwe studie onthult de ingrediënten van grote bosbranden Een auto van 1000 kg die 25 mijl per seconde in het oosten reist, heeft een botsing met een busje van 1500 kg in eerste instantie in rust met behoud van lineair momentum Wat is hun gemeenschappelijke snelheid onmiddellijk na de botsing?
Een auto van 1000 kg die 25 mijl per seconde in het oosten reist, heeft een botsing met een busje van 1500 kg in eerste instantie in rust met behoud van lineair momentum Wat is hun gemeenschappelijke snelheid onmiddellijk na de botsing?  Hoe stress werkt
Hoe stress werkt  De snelheid van het geluid door zuurstof bij 0 en ACIRC DEGC is 316 meter per seconde. Solid Copper 5010 Second.?
De snelheid van het geluid door zuurstof bij 0 en ACIRC DEGC is 316 meter per seconde. Solid Copper 5010 Second.?  Zeegrasherstel beter bestand maken tegen stijgende temperaturen met behulp van generalistische grassen
Zeegrasherstel beter bestand maken tegen stijgende temperaturen met behulp van generalistische grassen  Wat is het tegenovergestelde van Sky?
Wat is het tegenovergestelde van Sky?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


