
Wetenschap
Welk alkalimetaal reageert het meest langzaam met water?
Dit is waarom:
* kleiner formaat: Lithium is het kleinste alkalimetaal. Het kleinere formaat betekent dat het buitenste elektron nauwer wordt vastgehouden door de kern. Dit maakt het minder reactief in vergelijking met grotere alkali -metalen.
* Hogere ionisatie -energie: Lithium heeft een hogere ionisatie -energie dan de andere alkali -metalen. Dit betekent dat het meer energie vereist om het buitenste elektron te verwijderen, waardoor het minder snel deelneemt aan reacties met elektronenoverdracht, zoals de reactie met water.
Hoewel lithium wel met water reageert, doet het zoveel langzamer en met minder kracht dan natrium, kalium, rubidium en cesium.
 Wat maken tin en chloor?
Wat maken tin en chloor?  Is een zure elektronendonor?
Is een zure elektronendonor?  Maak een lijst van de drie soorten straling die tijdens het radioactieve decay
Maak een lijst van de drie soorten straling die tijdens het radioactieve decay Hoe beïnvloedt concentratie de reactiesnelheid?
Hoe beïnvloedt concentratie de reactiesnelheid?
Verhogen van de concentratie van reactanten verhoogt in het algemeen de reactiesnelheid omdat meer van de reagerende moleculen of ionen aanwezig zijn om de reactieproducten te vormen. Dit is vooral
 Woordvergelijking voor oplosbaar metaaloxide plus water?
Woordvergelijking voor oplosbaar metaaloxide plus water?
 Biologische voeding biedt aanzienlijke milieuvoordelen voor plantrijke diëten
Biologische voeding biedt aanzienlijke milieuvoordelen voor plantrijke diëten Hoe komt licht van de zon naar een object en dan onze ogen?
Hoe komt licht van de zon naar een object en dan onze ogen?  Groene mangoschil - een gladde oplossing voor met olie verontreinigde bodems
Groene mangoschil - een gladde oplossing voor met olie verontreinigde bodems Hoe socialebeschermingssystemen demografische veranderingen in Sub-Sahara Afrika faciliteren
Hoe socialebeschermingssystemen demografische veranderingen in Sub-Sahara Afrika faciliteren  Lava die uit de vulkaan Kilauea in Hawaï stroomt, vernietigt 9 huizen
Lava die uit de vulkaan Kilauea in Hawaï stroomt, vernietigt 9 huizen
Hoofdlijnen
- Hoe een van de X-chromosomen in vrouwelijke embryonale stamcellen tot zwijgen wordt gebracht
- Plaats deze in volgorde op grootte chromosoom kerncel -DNA en nucleotide?
- Wat zijn de vier stadia van evolutie?
- Wetenschappers onthullen hoe de 3D-schikking van DNA de soort helpt bestendigen
- Studie onderzoekt hoe de ruimtelijke verdeling van cellen in micro-omgevingen kan worden gecontroleerd
- Gemakkelijke manieren om botten te herkennen in anatomie
- GoT-ChA:Nieuw hulpmiddel onthult hoe genmutaties cellen beïnvloeden
- Analyse onderzoekt hoe religie en etniciteit de Aziatisch-Amerikaanse stemming bepalen
- Wat zijn gespecialiseerde structuren in een cel die specifieke functies uitvoeren?
- Technologie die eiwitstabiliteit voorspelt, is vrijgegeven door een spin-outbedrijf van een Britse universiteit

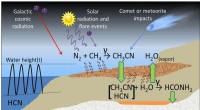
- Is het leven op waterbasis ontstaan zonder water?
- Klinische tests tonen aan dat biosensoren in de toekomst de weg kunnen effenen voor een gepersonaliseerde antibiotherapie

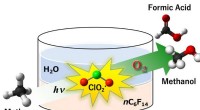
- Een radicale benadering van methaanoxidatie tot methanol
- Boeren en voedingsbedrijven gaan de strijd aan om de bodemgezondheid te verbeteren

 Uit welk mineraal is het skelet van diatomee bestaan?
Uit welk mineraal is het skelet van diatomee bestaan?  Onderzoekers ontdekken eerste enzymen die een klassieke organische reactie katalyseren
Onderzoekers ontdekken eerste enzymen die een klassieke organische reactie katalyseren Het zoutgehalte van de oceaan vanuit de ruimte volgen met behulp van kleur
Het zoutgehalte van de oceaan vanuit de ruimte volgen met behulp van kleur Hoeveel brandstof wordt verbrand op de hendellift van de shuttle?
Hoeveel brandstof wordt verbrand op de hendellift van de shuttle?  Wat gebeurt er als de zeespiegel stijgt en kustland onder water komt te staan?
Wat gebeurt er als de zeespiegel stijgt en kustland onder water komt te staan? Wat is er mis als er helemaal geen elektriciteit is gedurende een Geo -tracker?
Wat is er mis als er helemaal geen elektriciteit is gedurende een Geo -tracker?  Hoe een oudere ouder gunstig kan zijn voor het nageslacht
Hoe een oudere ouder gunstig kan zijn voor het nageslacht  Blijft de totale elektrische lading behouden bij negatief bètaverval?
Blijft de totale elektrische lading behouden bij negatief bètaverval?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

