
Wetenschap
Welk polyatomisch ion vormt een neutrale verbinding in combinatie met groep 1A monatomic in 1 2 verhouding?
Inzicht in de basis
* Groep 1A (Alkali metalen): Deze elementen hebben een +1 lading wanneer ze ionen vormen (bijv. Na+, K+, Li+).
* Polyatomische ionen: Dit zijn groepen atomen die werken als een enkele eenheid met een specifieke lading.
* Neutrale verbinding: Een verbinding met een netto lading van nul.
De logica
Om een neutrale verbinding te vormen met een 1:2 -verhouding (één groep 1a ion tot twee polyatomische ionen), moet het polyatomische ion een -1 -lading hebben. Dit komt omdat:
* Eén +1 lading van de groep 1a ion
* Twee -1 ladingen van de polyatomische ionen
* +1 + (-1) + (-1) =0 (een neutrale verbinding)
voorbeelden
Gemeenschappelijke polyatomische ionen met een -1 -lading zijn onder meer:
* hydroxide (oh-)
* nitraat (No3-)
* bicarbonaat (HCO3-)
Conclusie
Elk polyatomisch ion met een -1 lading zal een neutrale verbinding vormen met een groep 1A monatomisch ion in een verhouding van 1:2. Voorbeelden zijn:
* NaOH (natriumhydroxide)
* KNO3 (kaliumnitraat)
* LiHCO3 (lithium bicarbonaat)
 Bomen planten waar bossen waren?
Bomen planten waar bossen waren?  Coronavirus en bosbranden vormen samen een potentiële bedreiging voor inheemse levens en landen
Coronavirus en bosbranden vormen samen een potentiële bedreiging voor inheemse levens en landen Klimaat overgeleverd aan de politiek in 2020, experts waarschuwen
Klimaat overgeleverd aan de politiek in 2020, experts waarschuwen De CO2-kosten van thuisbezorging en hoe deze te vermijden
De CO2-kosten van thuisbezorging en hoe deze te vermijden Afvalmelk kan worden gebruikt om de uitstoot van kooldioxide in elektriciteitscentrales te verminderen
Afvalmelk kan worden gebruikt om de uitstoot van kooldioxide in elektriciteitscentrales te verminderen
Hoofdlijnen
- Hetzelfde gen, verschillende paringstechnieken bij vliegen
- Onderzoekers ontsluiten hoe cellen hun functies bepalen
- Welk eiwit wordt gemaakt in de plaveiselcel?
- Wat is het verschil tussen een opening en sluitspier?
- Wat is de naam van het proces waar materialen over een celmembraan worden verplaatst?
- Bevers kunnen wonderen doen voor de natuur, maar we moeten realistisch zijn over deze voordelen voor mensen
- Waarom leggen boomkikkers hun eieren op de grond?
- Wat is het ontwikkelingskind in de kiemstadium?
- Waarom kan multicellulair organisme complexer zijn dan eencellig gebruik van de drie kenmerken?
- Chemicus synthetiseert nieuwe verbindingen met sterke antidiabetische eigenschappen
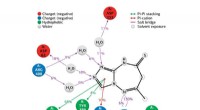
- Studie onthult structuur van receptor die betrokken is bij diabetes type 2 en meer
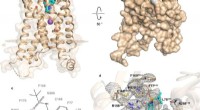
- Kleurafstembare, zeer mobiele emitterende organische eenkristallen voor lichtemitterende transistors

- Ontwikkeling van nieuwe fotovoltaïsche commercialiseringstechnologie

- Hydrofoob silica-colloïde-elektrolyt is veelbelovend voor veiligere lithium-zuurstofbatterijen
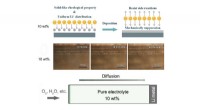
 Wat is CH3CH2O?
Wat is CH3CH2O?  Wat is de chemische naam van S04?
Wat is de chemische naam van S04?  Verbetering van de communicatie tussen koper en freelancer in de kluseconomie
Verbetering van de communicatie tussen koper en freelancer in de kluseconomie Wat zijn de 3 systemen met traktaten die met slijmvlies worden gevoerd?
Wat zijn de 3 systemen met traktaten die met slijmvlies worden gevoerd?  Wat is een geïsoleerde kei achtergelaten door een gletsjer?
Wat is een geïsoleerde kei achtergelaten door een gletsjer?  Wat is een ander woord voor het verbranden van fossiele brandstoffen?
Wat is een ander woord voor het verbranden van fossiele brandstoffen?  Wat is het doel van afgestudeerde cilinder bij het verzamelen van waterstofgas door waterverplaatsing?
Wat is het doel van afgestudeerde cilinder bij het verzamelen van waterstofgas door waterverplaatsing?  Facebook-vacatureservice verspreidt zich naar meer landen
Facebook-vacatureservice verspreidt zich naar meer landen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

