
Wetenschap
Welke van de volgende eigenschappen minimaliseert de verschillen tussen een ideaal gas en een echt gas?
* Ideale gasaannames: Het ideale gasmodel is gebaseerd op verschillende veronderstellingen, waaronder:
* Geen intermoleculaire krachten: Aangenomen wordt dat ideale gasmoleculen geen aantrekkingskracht of afstoting hebben.
* verwaarloosbaar moleculair volume: Het volume van de moleculen zelf wordt als onbeduidend beschouwd in vergelijking met het volume van de container.
* perfect elastische botsingen: Botsingen tussen moleculen worden verondersteld perfect elastisch te zijn, wat betekent dat er geen energie verloren gaat.
* echt gasgedrag: Echte gasmoleculen hebben intermoleculaire krachten en hun volume is niet te verwaarlozen. Bij hoge drukken en lage temperaturen worden deze factoren belangrijker:
* Hoge druk: Bij hoge druk zijn gasmoleculen dichter bij elkaar, waardoor het belang van intermoleculaire krachten vergroot.
* lage temperatuur: Bij lage temperaturen hebben moleculen minder kinetische energie, waardoor intermoleculaire krachten belangrijker worden.
* Minimalisatie van verschillen: Door te gaan naar lagere druk en hogere temperatuur:
* Lagere druk: Gasmoleculen liggen verder uit elkaar, waardoor de invloed van intermoleculaire krachten wordt verminderd.
* Hogere temperatuur: Moleculen hebben meer kinetische energie, waardoor hun volume te verwaarlozen is in vergelijking met de container en intermoleculaire krachten overwinnen.
Daarom zal het gedrag van een echt gas bij lage druk en hoge temperatuur het gedrag van een ideaal gas nauwer benaderen.
 Trump stelt openbaar land in Californië open voor fracking, gas leasen. Is het roekeloos?
Trump stelt openbaar land in Californië open voor fracking, gas leasen. Is het roekeloos? Programma's om seksueel geweld te voorkomen vertonen geen bewijs van het terugdringen van aanvallen, zo blijkt uit analyse
Programma's om seksueel geweld te voorkomen vertonen geen bewijs van het terugdringen van aanvallen, zo blijkt uit analyse  Gids uitgebracht ter ondersteuning van herstel na noodgevallen in Australië
Gids uitgebracht ter ondersteuning van herstel na noodgevallen in Australië Wat zijn de verschillende varianten van een gen genaamd?
Wat zijn de verschillende varianten van een gen genaamd?  Er komen aanwijzingen naar voren in het raadsel van ontbrekende plastic in de oceaan
Er komen aanwijzingen naar voren in het raadsel van ontbrekende plastic in de oceaan
Hoofdlijnen
- Wat wetenschapscommunicatoren zouden kunnen leren van marketingprofessionals
- Wat zijn abiotische dingen en biotische dingen?
- Vergelijking van klonen met mitose
- Gekruiste (evolutionaire) signalen?
- Economen ontwikkelen besluitvormingsmethode voor beheer van koraalduivels
- Waarom zwervende albatrossen scheiden:nieuw onderzoek
- Vleermuizen herbergen een gen dat afkomstig is van een eeuwenoud Ebola-achtig virus. Hier leest u hoe ze het kunnen gebruiken
- Wat is het doel van een fasciotomie?
- Wat bevindt zich buiten een celwand?
- Veranderingen in suikerachtige moleculen aan het oppervlak helpen kanker uitzaaien

- Moleculen uit moedermelk en zeewier suggereren strategieën voor het beheersen van norovirus
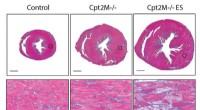
- Onderzoek toont aan dat vette brandstof nodig is om cardiale hypertrofie om te keren
- Upcyclingproces brengt nieuw leven in oude jeans

- Over het hele spectrum:onderzoekers vinden een manier om de kleur van licht in materiaal van de volgende generatie te stabiliseren

 Zuckerberg belooft te blijven bouwen in een adres zonder verontschuldiging
Zuckerberg belooft te blijven bouwen in een adres zonder verontschuldiging Welk deel van een atoom is positief geladen en welk deel negatief geladen?
Welk deel van een atoom is positief geladen en welk deel negatief geladen?  Geminiaturiseerde, zeer gevoelige ultrasone sensor voor fotoakoestische beeldvorming
Geminiaturiseerde, zeer gevoelige ultrasone sensor voor fotoakoestische beeldvorming Wat is het belang van chemicaliën in ons dagelijks leven?
Wat is het belang van chemicaliën in ons dagelijks leven?  Toch niet zo verschillend:menselijke cellen, winterharde microben delen een gemeenschappelijke voorouder
Toch niet zo verschillend:menselijke cellen, winterharde microben delen een gemeenschappelijke voorouder Programmeerbare structuren van de printer
Programmeerbare structuren van de printer Hoe werkt een zoemer in een elektrisch circuit?
Hoe werkt een zoemer in een elektrisch circuit?  Verstoren parasieten de voedselwebtheorie?
Verstoren parasieten de voedselwebtheorie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

