
Wetenschap
Welke dingen corroderen metaal?
Chemische reacties:
* oxidatie: Dit is de meest voorkomende vorm van corrosie, waarbij een metaal reageert met zuurstof in aanwezigheid van vocht of elektrolyten. Deze reactie vormt metaaloxiden, die vaak bros zijn en kunnen afvallen, waardoor het metaal wordt verzwakt. Roest op ijzer is een goed voorbeeld.
* zure aanval: Zuren kunnen metalen gemakkelijk aanvallen, vooral als ze sterk of geconcentreerd zijn. Dit kan gebeuren als gevolg van blootstelling aan zure regen, industriële verontreinigende stoffen of zelfs zure voedingsmiddelen.
* alkalische corrosie: Hoewel minder gebruikelijk, kunnen sterke alkalis ook bepaalde metalen corroderen. Beton bevat bijvoorbeeld alkali, waardoor stresscorrosiekraak in sommige staalsetijd kan veroorzaken.
Elektrochemische corrosie:
* Galvanische corrosie: Dit gebeurt wanneer twee ongelijksoortige metalen in contact staan met elkaar en een elektrolyt (zoals zout water). Het meer actieve metaal werkt als een anode en corrodeert, terwijl het minder actieve metaal werkt als een kathode en wordt beschermd.
* Crevice Corrosion: Dit type corrosie treedt op in smalle ruimtes of spleten waar zuurstof beperkt is. Het metaal in de spleet fungeert als een anode en corrodeert, terwijl het metaal buiten de spleet als een kathode fungeert.
* Putcorrosie: Dit is een gelokaliseerde vorm van corrosie die kleine gaten of kuilen in het metaaloppervlak creëert. Het komt vaak voor in stagnerende omgevingen waar een hoge concentratie opgeloste zouten is.
Omgevingsfactoren:
* vocht: Water is essentieel voor de meeste vormen van corrosie. Het werkt als een elektrolyt, waardoor ionen de elektrochemische reacties kunnen verplaatsen en faciliteren.
* Temperatuur: Hoge temperaturen kunnen corrosiesnelheden versnellen, omdat ze de snelheid van chemische reacties verhogen.
* verontreinigende stoffen: Industriële verontreinigende stoffen, zoals zwaveldioxide en stikstofoxiden, kunnen bijdragen aan corrosie door zure omgevingen te creëren.
* zout: Zoutwater is erg corrosief, omdat de opgeloste zouten fungeren als elektrolyten. Dit is de reden waarom mariene omgevingen bijzonder hard zijn voor metalen.
Andere factoren:
* Stress: Mechanische stress kan metalen gevoeliger maken voor corrosie, omdat het gebieden van hoge spanning creëert die het materiaal kunnen verzwakken.
* Micro -organismen: Sommige bacteriën en schimmels kunnen corrosie versnellen door corrosieve bijproducten te produceren.
Voorbeelden:
* IJzer Rusting: IJzer reageert met zuurstof en vocht om ijzeroxide (roest) te vormen.
* aluminium corrodeer: Aluminium vormt een beschermende oxidelaag die bestand is tegen verdere corrosie. In zure omgevingen kan deze laag echter afbreken en kan het aluminium corroderen.
* koper tarnishing: Koper reageert met zuurstof en zwavel in de lucht om een groene patina te vormen, wat een vorm van corrosie is.
Corrosie voorkomen:
* beschermende coatings: Het aanbrengen van verven, coatings of plating kan een barrière creëren tussen het metaal en de omgeving.
* Kathodische bescherming: Het gebruik van offersanodes of indruk op stroom om een kathodische omgeving te creëren en het metaal te beschermen.
* Materiaalselectie: Het kiezen van corrosiebestendige materialen zoals roestvrij staal of titanium.
* Omgevingscontrole: Het verminderen van de aanwezigheid van vocht, verontreinigende stoffen en andere corrosieve stoffen.
Inzicht in de oorzaken van corrosie is cruciaal om dit te voorkomen en de levensduur van metaalstructuren en componenten te waarborgen.
 Waarom is pH 10 voor het vinden van de hardheid van water. Iets gerelateerd aan protonatie?
Waarom is pH 10 voor het vinden van de hardheid van water. Iets gerelateerd aan protonatie?  Blokkeert het theeblokblok van ijzer?
Blokkeert het theeblokblok van ijzer?  Een stuk papier scheuren in de helft van de fysische of chemische verandering?
Een stuk papier scheuren in de helft van de fysische of chemische verandering?  Video:Eindelijk (peer-reviewed) chemie in wijn- en spijscombinaties
Video:Eindelijk (peer-reviewed) chemie in wijn- en spijscombinaties Hoe kan zinkchloride van siliciumoxide worden gescheiden?
Hoe kan zinkchloride van siliciumoxide worden gescheiden?
 Studie brengt stroomgebieden tussen stad en platteland in kaart en wijst op manieren om de beleids- en planningscoördinatie voor de landbouw te optimaliseren
Studie brengt stroomgebieden tussen stad en platteland in kaart en wijst op manieren om de beleids- en planningscoördinatie voor de landbouw te optimaliseren Hoe het madeliefje aan zijn vlekken kwam... en waarom
Hoe het madeliefje aan zijn vlekken kwam... en waarom  Naarmate de vraag naar EV's groeit, worden de sociale en ecologische risico's van lithiumgoudkoorts beoordeeld
Naarmate de vraag naar EV's groeit, worden de sociale en ecologische risico's van lithiumgoudkoorts beoordeeld Hoe mensen het ecosysteem ontwrichten
Hoe mensen het ecosysteem ontwrichten  Wat maakt een planeet bewoonbaar?
Wat maakt een planeet bewoonbaar?
Hoofdlijnen
- Hoe zorgt DNA -repliceren ervoor dat de continuïteit van vorm en functie van de ene celgeneratie naar de volgende zorgt?
- Wat is hypithese?
- Wat is een ander biologisch woord voor evenwicht?
- Waar worden lipiden gesynthetiseerd in eukaryoten?
- Wat is een soort bacteriën die in de darmen veel zoogdieren leeft?
- Hoe Bracket-schimmels aan hun eigen voedsel komen?
- Wetenschappers presenteren een nieuwe methode om elk eiwit in elk soort cel direct en snel te vernietigen
- Hoe leidde de biogenese theorie van de kiemaandoeningen?
- Waar of onwaar twee cellen geproduceerd tijdens de eerste cytokinese bij vrouwelijke dieren zijn ongeveer gelijke grootte en bevatten dezelfde hoeveelheid cytoplasma?
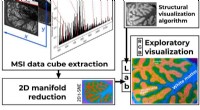
- Een nieuwe perceptueel consistente methode voor visualisatie van massaspectrometriebeeldvorming
- Video — Wijnsnobisme:feit versus fictie

- Zelfbevloeiende grond kan de landbouw transformeren

- Aan de lijn:kijken hoe nanodeeltjes vorm krijgen

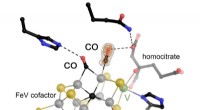
- Vanadiumafhankelijke stikstofase kan twee CO-moleculen tegelijk binden
 Inteelt en populatie/demografische verschuivingen kunnen hebben geleid tot het uitsterven van de Neanderthalers
Inteelt en populatie/demografische verschuivingen kunnen hebben geleid tot het uitsterven van de Neanderthalers Onderzoek onthult digitale impact op journalisten
Onderzoek onthult digitale impact op journalisten Ontbindende bladeren zijn een verrassende bron van broeikasgassen
Ontbindende bladeren zijn een verrassende bron van broeikasgassen Wat beïnvloedt de capaciteit van een geïsoleerde geleider?
Wat beïnvloedt de capaciteit van een geïsoleerde geleider?  Het biotricklingfilter ondersteunt een efficiënte waterstof-methaanconversie voor het opwaarderen van biologisch biogas
Het biotricklingfilter ondersteunt een efficiënte waterstof-methaanconversie voor het opwaarderen van biologisch biogas  Patronen van de maan
Patronen van de maan  Wetenschappers suggereren een nieuwe methode voor het synthetiseren van een veelbelovend magnetisch materiaal
Wetenschappers suggereren een nieuwe methode voor het synthetiseren van een veelbelovend magnetisch materiaal Afbeelding:Sentinel-1 ziet Mocoa aardverschuiving
Afbeelding:Sentinel-1 ziet Mocoa aardverschuiving
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

