
Wetenschap
Hoe is elektronegativiteit gerelateerd aan corrosie?
1. Elektrochemische cellen:
* Galvanische corrosie: Wanneer twee ongelijksoortige metalen met verschillende elektronegativiteiten in contact zijn in aanwezigheid van een elektrolyt (zoals water), wordt een elektrochemische cel gevormd.
* anode: Het metaal met lagere elektronegativiteit wordt de anode. Het verliest elektronen en ondergaat oxidatie en vormt metaalionen.
* kathode: Het metaal met hogere elektronegativiteit wordt de kathode. Het krijgt elektronen en ondergaat reductie, meestal van zuurstof- of waterstofionen.
* Corrosie: De anode corrodeert terwijl deze metaalionen verliest.
2. Standaard elektrodepotentiaal:
* Elektronegativiteit is direct gerelateerd aan de standaardelektrodepotentiaal van een metaal.
* Metalen met lagere elektronegativiteit hebben meer negatieve standaardelektrodepotentialen, wat duidt op een grotere neiging om elektronen te verliezen en oxidatie te ondergaan.
* Metalen met hogere elektronegativiteit hebben meer positieve standaardelektrodepotentialen, wat duidt op een mindere neiging om elektronen te verliezen en oxidatie te ondergaan.
3. Voorbeeld:
* Beschouw een stalen pijp (ijzer) in contact met een koperen fitting.
* IJzer heeft een lagere elektronegativiteit dan koper, waardoor het de anode is en meer vatbaar is voor corrosie.
* Koper wordt de kathode en is minder vatbaar voor corrosie.
* Dit is de reden waarom galvanische corrosie een zorg is wanneer ongelijksoortige metalen in contact zijn, vooral in aanwezigheid van vocht.
4. Andere factoren die corrosie beïnvloeden:
* omgeving: Temperatuur, vochtigheid, pH en aanwezigheid van agressieve chemicaliën kunnen alle corrosiesnelheden beïnvloeden.
* metaaloppervlak: Oppervlakte -onvolkomenheden, spanningsconcentraties en coatings kunnen de initiatie en voortplanting van corrosie beïnvloeden.
Samenvattend:
* Elektronegativiteit is een fundamentele eigenschap die rechtstreeks de neiging van een metaal beïnvloedt om te corroderen.
* Metalen met lagere elektronegativiteit zijn eerder anodes en ondergaan oxidatie, wat leidt tot corrosie.
* Het verschil in elektronegativiteit tussen twee metalen in contact is een sleutelfactor bij het bepalen van de ernst van galvanische corrosie.
 Andrew was een monster; Irma zou het uit het water kunnen blazen
Andrew was een monster; Irma zou het uit het water kunnen blazen Nieuw onderzoek werpt licht op de extreme weersomstandigheden in 2020 die branden en sneeuw naar het westen van de VS brachten
Nieuw onderzoek werpt licht op de extreme weersomstandigheden in 2020 die branden en sneeuw naar het westen van de VS brachten  Wat een opwarmende wereld betekent voor dodelijke tornado's en het soort stormen dat ze voortbrengt
Wat een opwarmende wereld betekent voor dodelijke tornado's en het soort stormen dat ze voortbrengt  Hoe de regelgeving van atrazine het milieu heeft beïnvloed
Hoe de regelgeving van atrazine het milieu heeft beïnvloed Het is meer dan alleen klimaatverandering
Het is meer dan alleen klimaatverandering
Hoofdlijnen
- Systeem dat reproductie mogelijk maakt en mannelijke vrouwelijke functies in staat stelt?
- Wat zijn plasmiden en hoe kunnen ze worden gebruikt om transgene organismen te creëren?
- Hoe eiwitten influenza A helpen zich te binden en zich een weg te banen naar cellen
- Hoe komen de wetenschappers ten goede aan de samenleving?
- Onderzoekers ontdekken hoe CRISPR/Cas vreemd DNA steelt voor het bacteriële immuunsysteem
- Wat is de rol van zijderupsen in het ecosysteem?
- Wat is de taak van het Golgi -apparaat in een bacteriecel?
- Hoe de eenvoudige goudsbloem een verwoestende tomatenplaag te slim af is
- Wat zijn de drie soorten grenzen in de wetenschap?
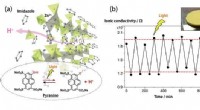
- Protongeleiding regelen met licht
- Een onwaarschijnlijk huwelijk tussen oxiden

- Veelzijdig moleculair systeem vergroot de belofte van door licht geactiveerde schakelaars

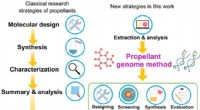
- Het ontwerpen van krachtige hypergolische drijfgassen voor ruimteraketten op basis van het materiaalgenoom
- Ongebruikelijke suiker van cyanobacteriën werkt als natuurlijk herbicide

 Wat is de werking van natriumhydroxide op kleur rode lakmoes?
Wat is de werking van natriumhydroxide op kleur rode lakmoes?  Nieuw onderzoek laat zien hoeveel voedsel zeevogels nodig hebben
Nieuw onderzoek laat zien hoeveel voedsel zeevogels nodig hebben  Robots leren sneller met kwantumtechnologie
Robots leren sneller met kwantumtechnologie Hoe nieuwe ontwerppatronen steden en hun bewoners in staat kunnen stellen te veranderen met klimaatverandering
Hoe nieuwe ontwerppatronen steden en hun bewoners in staat kunnen stellen te veranderen met klimaatverandering Waarom is de vorming van uni-negatief ionen een exothermiisch proces?
Waarom is de vorming van uni-negatief ionen een exothermiisch proces?  Wat zijn de 4 belangrijkste groepen algen?
Wat zijn de 4 belangrijkste groepen algen?  Watervallen bieden inzicht in hoe rivieren hun omgeving vormgeven
Watervallen bieden inzicht in hoe rivieren hun omgeving vormgeven 6ft 8 in is gelijk aan hoeveel cm?
6ft 8 in is gelijk aan hoeveel cm?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

