
Wetenschap
Wat doet zeep met de polariteit van een watermolecuul?
* Polariteit van het water: Watermoleculen zijn inherent polair. Ze hebben een gebogen vorm waarbij zuurstof meer elektronegatief is dan waterstof, waardoor een gedeeltelijke negatieve lading aan de zuurstofzijde en gedeeltelijke positieve ladingen aan de waterstofzijde ontstaan. Deze polariteit is fundamenteel voor de eigenschappen van het water.
* Soap's rol: Soapmoleculen zijn amfifiel, wat betekent dat ze zowel hydrofiele (waterminnende) als hydrofobe (watervullende) uiteinden hebben.
* Het hydrofiele uiteinde wordt aangetrokken door watermoleculen en lost op in water.
* Het hydrofobe uiteinde wordt afgestoten door water en aangetrokken tot oliën en vet.
* Hoe zeep werkt: Soap werkt door de krachten te verstoren die olie vasthouden en samenvoegen. De hydrofobe staarten van zeepmoleculen omringen het olie/vet en vormen micellen. De hydrofiele koppen van de zeepmoleculen wijzen naar buiten, waardoor de micellen zich in water kunnen verspreiden en weg kunnen worden weggespoeld.
Samenvattend: Zeep verandert de polariteit van watermoleculen niet. In plaats daarvan gebruikt het zijn eigen amfifiele aard om te interageren met zowel water- als niet-polaire stoffen, waardoor vet en vuil effectief wordt schoongemaakt en verwijderd.
 Wat is de hardheid van een wasmachine van klasse 2?
Wat is de hardheid van een wasmachine van klasse 2?  Reageert ijzer met chloor en vormt chloride?
Reageert ijzer met chloor en vormt chloride?  Waarom moeten meststoffen oplosbaar zijn in water?
Waarom moeten meststoffen oplosbaar zijn in water?  Wetenschappers ontwikkelen een katalysator die is ontworpen om de productie van ammoniak duurzamer te maken
Wetenschappers ontwikkelen een katalysator die is ontworpen om de productie van ammoniak duurzamer te maken  Wat is de chemische vergelijking voor natriumwaterstofcarbonaat en limwater?
Wat is de chemische vergelijking voor natriumwaterstofcarbonaat en limwater?
 Orkanen voorkomen met luchtbellen
Orkanen voorkomen met luchtbellen Wat de stijgende zeeën betekenen voor lokale economieën
Wat de stijgende zeeën betekenen voor lokale economieën Canada faalt in strijd tegen klimaatverandering:waakhond
Canada faalt in strijd tegen klimaatverandering:waakhond Uit onderzoek blijkt hoe een hoge spar een verdedigingsmechanisme ontwikkelt tegen hongerige snuitkevers
Uit onderzoek blijkt hoe een hoge spar een verdedigingsmechanisme ontwikkelt tegen hongerige snuitkevers  Oude beschavingen hadden manieren om het stedelijke hitte-eilandeffect tegen te gaan:hoe de lessen uit de geschiedenis hedendaagse steden toepassen
Oude beschavingen hadden manieren om het stedelijke hitte-eilandeffect tegen te gaan:hoe de lessen uit de geschiedenis hedendaagse steden toepassen
Hoofdlijnen
- Waarom gebruiken cellen GTP in plaats van ATP bij celsignalering?
- Vogelgriep:hoe het zich verspreidt en wat u moet weten over deze uitbraak
- Hoeveel van onze hersenen gebruiken we? De mythe ontkrachten
- Hoe kan het weten dat plantencellen chloroplasten hebben en dieren u niet helpen de manier waarop planten voedsel krijgen te vergelijken?
- Wat wordt het proces dat wordt genoemd door welke wetenschapper controleert of anderen eerder werken in publicatiewetenschappelijke tijdschriften?
- Hoe leg je de test uit?
- Waarom geven we de voorkeur aan bepaalde voedingsmiddelen boven andere?
- Hoe zijn de verdeeldheid tussen cellen in veel schimmels genaamd-?
- Wat voor soort stamcellen kunnen zich in het menselijk lichaam ontwikkelen?
- Nieuw isolatiemateriaal zorgt voor een efficiëntere elektriciteitsdistributie

- Wetenschappers ontdekken nieuw type zelfherstellend materiaal
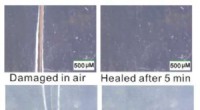
- Slimme materialen die in ultrageluid worden gebruikt, gedragen zich vergelijkbaar met water, chemici melden

- Nieuwe studies van oud beton zouden ons kunnen leren te doen zoals de Romeinen deden

- Waardoor smaakt en ruikt de Appalachian truffel heerlijk?

 Brazilië heeft twee populaties Amerikaanse brulkikkers, een exotische soort die een dodelijke schimmel overdraagt
Brazilië heeft twee populaties Amerikaanse brulkikkers, een exotische soort die een dodelijke schimmel overdraagt Is de moleculaire massa kaarsenwas minder dan 100?
Is de moleculaire massa kaarsenwas minder dan 100?  Hoe beïnvloeden uw hersenen de overlevingskansen in de wildernis?
Hoe beïnvloeden uw hersenen de overlevingskansen in de wildernis?  Hoe Factor Met Negatieve Fractionele Exponenten
Hoe Factor Met Negatieve Fractionele Exponenten  Een 3D-camera voor veiligere autonomie en geavanceerde biomedische beeldvorming
Een 3D-camera voor veiligere autonomie en geavanceerde biomedische beeldvorming India's erfgoedstad racet om iconen te redden van vervuilde ruïne
India's erfgoedstad racet om iconen te redden van vervuilde ruïne Zijn sommige sterren ongeveer zo kleine aarde?
Zijn sommige sterren ongeveer zo kleine aarde?  Is lucht verzegeld in een pot gas?
Is lucht verzegeld in een pot gas?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

