
Wetenschap
Wat zijn edelgasconfiguraties?
Nobele gasconfiguraties:een stabiele staat van atomen
Nobele gasconfiguraties verwijzen naar de elektronenopstelling van atomen die lijken op de stabiele configuratie van edelgassen. Deze gassen, gelegen in groep 18 van de periodiek systeem (helium, neon, argon, Krypton, Xenon en Radon), zijn ongelooflijk niet -reactief vanwege hun volledige buitenste elektronenschalen .
Hier is een uitsplitsing van het concept:
1. Elektronenschalen en subshells:
- Atomen hebben elektronen die in een baan om hun kern draaien in verschillende energieniveaus die shells worden genoemd .
- Elke schaal kan een bepaald maximaal aantal elektronen bevatten.
- Shells zijn verder onderverdeeld in subshells , aangeduid als S, P, D en F, waarbij elk specifieke elektronencapaciteiten heeft.
2. Nobele gasconfiguratie:
- Nobele gassen hebben een volledige buitenste elektronenschil, wat betekent dat al hun subschalen gevuld zijn met het maximale aantal elektronen.
- Deze stabiele configuratie maakt ze extreem niet -reactief.
3. Het bereiken van edelgasconfiguratie:
- Andere elementen streven ernaar om een edelgasconfiguratie te bereiken door elektronen te verkrijgen, te verliezen of te delen door chemische binding.
- Deze neiging stimuleert chemische reacties en vormt de basis van chemische bindingstheorieën.
4. Notatie van edelgas gebruiken:
- Noble Gas Notation is een steno manier om elektronenconfiguraties te schrijven.
- Het gebruikt het symbool van het vorige edelgas gevolgd door de elektronenconfiguratie van de resterende elektronen.
- Natrium (NA) heeft bijvoorbeeld 11 elektronen. De elektronenconfiguratie is 1S²2S²2P⁶3S¹. Met behulp van edelgasnotatie schrijven we het als [ne] 3s¹. Dit betekent dat natrium dezelfde elektronenconfiguratie heeft als neon (1S²2S²2P⁶) plus één extra elektron in de 3S -subshell.
5. Belang van edelgasconfiguratie:
- Het begrijpen van edelgasconfiguraties helpt de reactiviteit en het chemische gedrag van elementen te voorspellen.
- Het biedt een raamwerk voor het verklaren van chemische binding en de vorming van verbindingen.
- Het is een fundamenteel concept in de chemie dat helpt de structuur en eigenschappen van materie te begrijpen.
Concluderend vertegenwoordigen edelgasconfiguraties de stabiele toestand van atomen, waarbij hun buitenste schalen volledig gevuld zijn met elektronen. Inzicht in dit concept is cruciaal voor het grijpen van de principes van chemische binding en het gedrag van elementen in chemische reacties.
 Wat is een mengsel waar de stof niet gemakkelijk van elkaar kan worden onderscheiden?
Wat is een mengsel waar de stof niet gemakkelijk van elkaar kan worden onderscheiden?  Hoe noemen we kleinere deeltjes die samen een chloormolecuul vormen?
Hoe noemen we kleinere deeltjes die samen een chloormolecuul vormen?  Hoe moleculen bewegen in elk van de drie staten is belangrijk?
Hoe moleculen bewegen in elk van de drie staten is belangrijk?  Wat zijn roodachtige gaslussen die verschillende onderdelen Sunspots verbinden?
Wat zijn roodachtige gaslussen die verschillende onderdelen Sunspots verbinden?  Moeilijk, sterk en hittebestendig:bio-geïnspireerd materiaal ter vervanging van plastic
Moeilijk, sterk en hittebestendig:bio-geïnspireerd materiaal ter vervanging van plastic
Hoofdlijnen
- Waarom zijn protines belangrijk voor de cellulaire functie?
- Hoe bacteriën eiwitten exploiteren om potentieel dodelijke infecties te veroorzaken
- Voorbeelden van sensorische aanpassing
- Wat zijn de drie macromoleculen die uw lichaam nodig heeft voor een goede voeding?
- Hoe rockagama's slaapplekken in steden uitkiezen
- Wat is een basisprincipe van kinesiologie?
- Waarom zijn er geen zeeslangen in de Atlantische Oceaan?
- Wat wordt er gevormd uit gametophytes?
- Kunnen we ons een weg banen door een exploderend zee-egelprobleem?
- Onderzoekers ontwikkelen snelle en eenvoudige methode voor glyfosaatdetectie

- Collageenstructuren krijgen de koninklijke onthulling
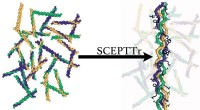
- Onderzoekers creëren een nieuwe klasse van snelheidsgevoelige mechanische metamaterialen

- PFAS-chemicaliën gaan niet eeuwig mee
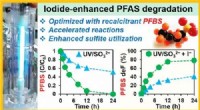
- De limieten van Li-ion-batterijen uitbreiden - elektroden voor volledig solid-state batterijen
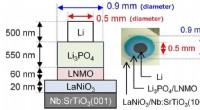
 Wetenschappers demonstreren met hoge resolutie dat lidar de geboortezone van wolkendruppeltjes ziet, een allereerste observatie op afstand
Wetenschappers demonstreren met hoge resolutie dat lidar de geboortezone van wolkendruppeltjes ziet, een allereerste observatie op afstand  Versnelling van ijsverlies op Groenland
Versnelling van ijsverlies op Groenland Technologie stijgt in het bevorderen van kritische communicatie, veiligheid voor piloten, passagiers
Technologie stijgt in het bevorderen van kritische communicatie, veiligheid voor piloten, passagiers Hoe maak je een model van de moleculaire structuur van Water
Hoe maak je een model van de moleculaire structuur van Water Hoe voelen ziekteverwekkers de omgeving? Wetenschappers identificeren de structuren van belangrijke eiwitten
Hoe voelen ziekteverwekkers de omgeving? Wetenschappers identificeren de structuren van belangrijke eiwitten  Sleutelexperiment bij 's werelds grootste atom-smasher krijgt upgrade
Sleutelexperiment bij 's werelds grootste atom-smasher krijgt upgrade Naam 3 items gevonden in de ruimte naast sterren Moonets?
Naam 3 items gevonden in de ruimte naast sterren Moonets?  Optisch keramiek ontmoet metaal-organische kaders
Optisch keramiek ontmoet metaal-organische kaders
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

