
Wetenschap
Hoe wordt een covalente binding gevormd tussen twee broomatomen?
1. Inzicht in de eigenschappen van Bromine:
* valentie -elektronen: Bromine (BR) heeft 7 valentie -elektronen (elektronen in de buitenste schaal).
* stabiliteit: Atomen proberen een volledige buitenste schaal van elektronen (8 voor de meeste atomen) te hebben voor stabiliteit.
2. Het bindproces:
* Elektronen delen: Om een stabiele configuratie te bereiken, delen twee broomatomen elk één elektron. Dit gedeelde paar elektronen vormt de covalente binding.
* Moleculaire orbitale vorming: Wanneer de twee atomaire orbitalen (één van elk broomatoom) elkaar overlappen, vormen ze een nieuw, moleculair lagere orbitaal. De gedeelde elektronen bezetten dit moleculaire orbitaal, wat resulteert in een sterkere, stabielere opstelling.
* Niet -polaire covalente binding: Omdat beide broomatomen dezelfde elektronegativiteit hebben (vermogen om elektronen aan te trekken), zijn de gedeelde elektronen gelijk verdeeld tussen hen. Dit maakt de binding niet -polair.
3. Visuele weergave:
* Lewis -structuur: De binding wordt weergegeven door een enkele lijn die de twee broommogelijkheden verbindt:
`` `
Br - Br
`` `
* Elektronenstipdiagram: Dit toont de valentie -elektronen en het gedeelde paar:
`` `
:Br. .Br:
| |
| |
| |
:Br. .Br:
`` `
Samenvattend: Een covalente binding tussen twee broomatomen wordt gevormd door een paar elektronen te delen, wat resulteert in een stabiel molecuul met een niet -polaire covalente binding.
 Actieve kool kan leiden tot geurloze luiers
Actieve kool kan leiden tot geurloze luiers Voorbeelden van andere niet-mengbare vloeistoffen dan olie?
Voorbeelden van andere niet-mengbare vloeistoffen dan olie?  Onderzoek brengt vroege ziekteverschijnselen in de schijnwerpers met infraroodlicht
Onderzoek brengt vroege ziekteverschijnselen in de schijnwerpers met infraroodlicht Wat zijn twee redenen waarom dichtheid een nuttige eigenschap is voor het identificeren van stoffen?
Wat zijn twee redenen waarom dichtheid een nuttige eigenschap is voor het identificeren van stoffen?  Brazilianen creëren een sensor om de niveaus van veelgebruikte antibiotica in water en voedsel te monitoren
Brazilianen creëren een sensor om de niveaus van veelgebruikte antibiotica in water en voedsel te monitoren
 Ruimtetechnologie toevoegen aan de waterbehoeften in de wijngaarden van Californië
Ruimtetechnologie toevoegen aan de waterbehoeften in de wijngaarden van Californië Herten kunnen COVID vangen:dit is wat jagers moeten weten
Herten kunnen COVID vangen:dit is wat jagers moeten weten  Sommige voedselverontreiniging begint in de bodem
Sommige voedselverontreiniging begint in de bodem Wat is er ter wereld die je ziet, maar het kan ruiken?
Wat is er ter wereld die je ziet, maar het kan ruiken?  Door NASA gebouwd instrument helpt superstralers van broeikasgassen op te sporen
Door NASA gebouwd instrument helpt superstralers van broeikasgassen op te sporen
Hoofdlijnen
- Vervangt uw lichaam zichzelf echt elke zeven jaar?
- Nieuwe studie wijst op onverwachte voordelen van rabiësvaccinatie bij honden
- Wat gebruikt de proceswetenschapper om informatie te verzamelen?
- Waarom meiose 2 vergelijkbaar is met mitose?
- Belang van vrije ribosomen
- Wie zijn sciencetist?
- Atrazine verandert de sex-ratio in Blanchards krekelkikkers
- Wat voor soort molecuul is aanwezig in een celmembraan?
- Wat levert bloed af aan elk deel van het lichaam?
- Leren van de rijkdom van de natuur:nieuwe bibliotheken voor het ontdekken van medicijnen
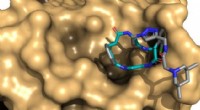
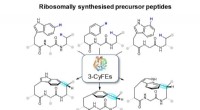
- Onderzoekers identificeren post-translationele vorming van gespannen cyclofanen in bacteriën
- Waterstofkracht komt een stap dichterbij

- Hoogrenderende thermo-elektrische materialen:nieuwe inzichten in tinselenide
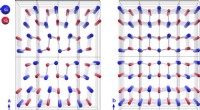
- Sommigen houden van cryogeen

 Hoe LISA Pathfinder tientallen 'komeetkruimels' ontdekte
Hoe LISA Pathfinder tientallen 'komeetkruimels' ontdekte  Hoe kun je de datum kennen waarin levende dingen op aarde bestonden?
Hoe kun je de datum kennen waarin levende dingen op aarde bestonden?  Onderzoekers voeren een uitgebreid onderzoek uit naar de bereiding van op MOF gebaseerde vlamvertragers via coördinatiebindingssplitsing
Onderzoekers voeren een uitgebreid onderzoek uit naar de bereiding van op MOF gebaseerde vlamvertragers via coördinatiebindingssplitsing  Wat voor soort eenvoudige machine is een beker?
Wat voor soort eenvoudige machine is een beker?  Sommigen houden van cryogeen
Sommigen houden van cryogeen Welke omvang van de ster is helderder -5 of 2?
Welke omvang van de ster is helderder -5 of 2?  Leidt meer onderwijs tot politiek geweld?
Leidt meer onderwijs tot politiek geweld? Wat is de wiskundige relatie tussen lading en coulombkracht?
Wat is de wiskundige relatie tussen lading en coulombkracht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

