
Wetenschap
Waarom zijn de formules van bariumchloride en strontium vergelijkbaar?
* Bevat een metaal uit dezelfde groep: Zowel barium (BA) als Strontium (SR) bevinden zich in groep 2 van het periodiek systeem, ook bekend als de alkalische aardmetalen. Dit betekent dat ze allebei twee valentie -elektronen hebben, waardoor ze zeer reactief zijn en vatbaar zijn voor het verliezen van die twee elektronen om een +2 lading te vormen.
* Combineer met hetzelfde niet-metaal: Beide verbindingen bevatten chloor (CL), een halogeen in groep 17. Chloor heeft een hoge elektronegativiteit en heeft de neiging om één elektron te krijgen om een -1 -lading te vormen.
Vorming van de verbindingen:
* Bariumchloride (BACL₂): Barium (ba²⁺) verliest twee elektronen om een +2 kation te vormen. Chloor (CL⁻) krijgt één elektron om een -1 anion te vormen. Om de ladingen in evenwicht te brengen, zijn twee chloride -ionen nodig voor elk bariumion, resulterend in de formule BACL₂.
* strontiumchloride (srcl₂): Strontium (Sr²⁺) verliest ook twee elektronen om een +2 kation te vormen. Nogmaals, er zijn twee chloride -ionen (CL⁻) nodig om elk strontium -ion in evenwicht te brengen, waardoor de formule SRCL₂ wordt gegeven.
In wezen komt de gelijkenis in hun formules voort uit de vergelijkbare chemische eigenschappen van barium en strontium, beide vormen +2 kationen en combineren met chloride -ionen in een verhouding van 1:2.
 Is string een vast of vloeibaar gas?
Is string een vast of vloeibaar gas?  Wat is de chemische formule voor koper I fosfaat?
Wat is de chemische formule voor koper I fosfaat?  Welk proces kan worden gebruikt om kaliumchloride te zuiveren?
Welk proces kan worden gebruikt om kaliumchloride te zuiveren?  Putty-achtige composieten van galliummetaal met potentieel voor toepassing in de echte wereld
Putty-achtige composieten van galliummetaal met potentieel voor toepassing in de echte wereld Er zit 2 gram H2-gas in een container met een vast volume van 273 C. 16 Hij wordt toegevoegd aan de en de temperatuur wordt verhoogd 819 Dus welke verhouding einddruk begindruk?
Er zit 2 gram H2-gas in een container met een vast volume van 273 C. 16 Hij wordt toegevoegd aan de en de temperatuur wordt verhoogd 819 Dus welke verhouding einddruk begindruk?
 Wat is het verste object op aarde dat een persoon zonder hulp kan zien?
Wat is het verste object op aarde dat een persoon zonder hulp kan zien?  Kunnen drijvende steden mensen helpen zich aan te passen aan de stijgende zeespiegel?
Kunnen drijvende steden mensen helpen zich aan te passen aan de stijgende zeespiegel? Wat is de wetenschappelijke definitie voor Strong?
Wat is de wetenschappelijke definitie voor Strong?  Wat zijn enkele planten en dieren die specifiek zijn in Noord -Amerika Midden -Zuid -Amerika?
Wat zijn enkele planten en dieren die specifiek zijn in Noord -Amerika Midden -Zuid -Amerika?  Wat is jouw omgeving?
Wat is jouw omgeving?
Hoofdlijnen
- Waar trekt plasma -eiwitsynthese op?
- Wetenschappers stellen efficiëntieregels voor om het gebruik van nieuwe technologie voor het bewerken van genen te verbeteren
- Onderzoekers beschrijven een belangrijk onderdeel in het energievoorzieningsmechanisme van het lichaam
- Wat is een eigenschap waarmee een organisme beter kan overleven of zich beter voortplant dan anderen zonder de in specifieke omgeving?
- Wat is de klasse voor dieren?
- Een tand terug laten groeien? Vis – ja; mensen – misschien ooit
- Is Archaea een producent consumenten of ontcomposer?
- Studie decodeert dimerisatie en herkenning van antidepressiva op de noradrenalinetransporteur
- Welk eiwit vormt microtubuli in de cel?
- Studie biedt nieuwe inzichten voor technologieën voor het verzamelen van de zon

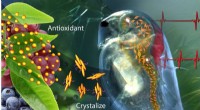
- Slim antioxidant-bevattend polymeer reageert op lichaamschemie, omgeving
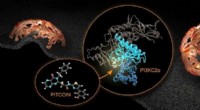
- Remmer van lipidekinase PI3KC2a geïdentificeerd als potentiële nieuwe behandeling van trombose
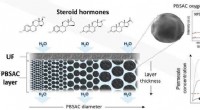
- Efficiënte verwijdering van steroïde hormonen uit water
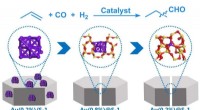
- Onderzoekers ontwikkelen nieuwe Au-katalysator voor hydroformylering
 Observatie tijdens de reactie van strontium en zuurstof?
Observatie tijdens de reactie van strontium en zuurstof?  Hoe olie te distilleren met behulp van een koffiepot
Hoe olie te distilleren met behulp van een koffiepot  Wat is de vaste stof die overblijft na het verwarmen van steenkool of benzine?
Wat is de vaste stof die overblijft na het verwarmen van steenkool of benzine?  Nieuw onderzoek laat zien hoe AI ons kan helpen de mondiale bedreigingen voor wilde dieren beter te begrijpen
Nieuw onderzoek laat zien hoe AI ons kan helpen de mondiale bedreigingen voor wilde dieren beter te begrijpen  De reis van een dodenmasker van de Duitse toneelschrijver Frank Wedekind
De reis van een dodenmasker van de Duitse toneelschrijver Frank Wedekind In welke fase is de maan als deze volledig verlicht lijkt, zoals een gloeiende orb -nachthemel?
In welke fase is de maan als deze volledig verlicht lijkt, zoals een gloeiende orb -nachthemel?  Cellulosevezels zijn in opkomst als duurzame optie voor het verpakken van alles, van voedsel tot elektronica
Cellulosevezels zijn in opkomst als duurzame optie voor het verpakken van alles, van voedsel tot elektronica  Onderzoekers op weg om krachtige en praktische kwantumcomputer te bouwen
Onderzoekers op weg om krachtige en praktische kwantumcomputer te bouwen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

