
Wetenschap
Hoe beïnvloedt de temperatuur de oplosbaarheid van de meeste vaste stoffen?
Dit is waarom:
* Kinetische energie: Naarmate de temperatuur toeneemt, krijgen de moleculen in zowel de vaste stof als de vloeistof meer kinetische energie. Dit betekent dat ze sneller bewegen en vaker botsen.
* Breaking Bonds: De verhoogde kinetische energie helpt de krachten te overwinnen die de moleculen van de vaste stof bij elkaar houden (de roosterstructuur), waardoor het gemakkelijker is om uit elkaar te breken en op te lossen in de vloeistof.
* Verhoogde interactie: De sneller bewegende moleculen van zowel de vaste stof als de vloeistof interageren vaker en met een grotere kracht, wat leidt tot een grotere oplossing.
Uitzonderingen:
Hoewel dit over het algemeen waar is, zijn er enkele uitzonderingen:
* gassen: De oplosbaarheid van gassen in vloeistoffen * neemt * af * met toenemende temperatuur. Dit komt omdat hogere temperaturen ervoor zorgen dat gasmoleculen gemakkelijker uit de vloeistof ontsnappen.
* Bepaalde zouten: Een paar zouten, zoals lithiumsulfaat (li₂so₄), worden eigenlijk * minder * oplosbaar naarmate de temperatuur stijgt.
Belangrijke opmerking:
Het specifieke effect van de temperatuur op oplosbaarheid kan variëren, afhankelijk van de specifieke vaste vaste stof en vloeistof. Over het algemeen maakt het verhogen van de temperatuur het echter gemakkelijker voor de meeste vaste stoffen om op te lossen.
 Welke getallen en mineralen op de hardheidsschaal van Mohs zijn waar of onwaar?
Welke getallen en mineralen op de hardheidsschaal van Mohs zijn waar of onwaar?  Onderzoekers ontwikkelen hoogwaardige keramische brandstofcel die werkt op butaangas
Onderzoekers ontwikkelen hoogwaardige keramische brandstofcel die werkt op butaangas Nutriënten tegen kanker in slabladeren nemen toe tijdens de houdbaarheid na de oogst
Nutriënten tegen kanker in slabladeren nemen toe tijdens de houdbaarheid na de oogst Welke heeft meer massa een stikstofmolecuul of een zuurstofmolecuul?
Welke heeft meer massa een stikstofmolecuul of een zuurstofmolecuul?  Wat zijn de eigenschappen van ophanging in de chemie?
Wat zijn de eigenschappen van ophanging in de chemie?
 Hoe oeverbuffers werken om uw lokale waterwegen te redden
Hoe oeverbuffers werken om uw lokale waterwegen te redden  Nieuw onderzoek laat zien hoe vleermuizen 's nachts hun weg naar huis 'haasten'
Nieuw onderzoek laat zien hoe vleermuizen 's nachts hun weg naar huis 'haasten'  Onderzoek suggereert dat hittegolven tijdens de kindertijd een negatief effect kunnen hebben op het inkomen van volwassenen
Onderzoek suggereert dat hittegolven tijdens de kindertijd een negatief effect kunnen hebben op het inkomen van volwassenen Wat verwijst naar de warmte of kou van een object?
Wat verwijst naar de warmte of kou van een object?  Wat is het verschil tussen een bergketen en systeem?
Wat is het verschil tussen een bergketen en systeem?
Hoofdlijnen
- Resultaten van Landmark NASA DNA Twin Study zijn binnen
- Waarom is de kern belangrijk voor een levende cel?
- In welke tak van de wetenschap is Bill Gates?
- Wat is ATP wat zijn functie?
- Wat beschrijft het beste waar cellulaire ademhaling?
- Niet alle dieren in het wild zijn hersteld in lockdowns, zo blijkt uit nieuw onderzoek
- Op welke manieren verschillen de chemische structuren van DNA en RNA?
- Wie zijn zes mensen die bijdragen hebben geleverd op het gebied van genetica?
- Definieer Contrast in microscopen
- Nieuwe synthetische methode voor waterstabiele perovskieten

- Enzymontdekking kan helpen bij de bestrijding van tuberculose

- Ontwerpen van selectieve membranen voor batterijen met behulp van een toolbox voor het ontdekken van medicijnen
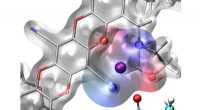
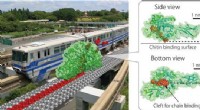
- Chitinase als verbrande brug Brownse monorail die op efficiënte wijze recalcitrante biomassa hydrolyseert
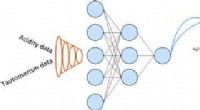
- Chemici leren neurale netwerken om eigenschappen van verbindingen te voorspellen
 Gemiddelde mensen kunnen het verschil maken bij mondiale uitdagingen, zegt onderzoeker
Gemiddelde mensen kunnen het verschil maken bij mondiale uitdagingen, zegt onderzoeker Taiwan getroffen door meer naschokken
Taiwan getroffen door meer naschokken Wat lost het oplosmiddel of opgeloste stof op?
Wat lost het oplosmiddel of opgeloste stof op?  Hoeveel AU is alpha centauri van de aarde?
Hoeveel AU is alpha centauri van de aarde?  Nieuwe komeet NEOWISE siert de lucht
Nieuwe komeet NEOWISE siert de lucht Welk vliegtuig heeft de grootste maan?
Welk vliegtuig heeft de grootste maan?  Kun je later in je leven ambidexter worden? Het hangt ervan af
Kun je later in je leven ambidexter worden? Het hangt ervan af  Wat is kunstmatige fokkerij?
Wat is kunstmatige fokkerij?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

