
Wetenschap
Wat gebeurt er als u waterstofionen toevoegt aan een neutrale oplossing?
* pH -schaal: De pH -schaal meet de zuurgraad of alkaliteit van een oplossing. Het varieert van 0 tot 14, met:
* 0-6.9: Zuur
* 7: Neutrale
* 7.1-14: Basis (alkalisch)
* waterstofionen en pH: De concentratie waterstofionen (H+) in een oplossing bepaalt de pH. Hoe hoger de concentratie van H+, hoe lager de pH en hoe zure de oplossing.
* Neutrale oplossing: Een neutrale oplossing heeft een gelijke concentratie van H+ en hydroxide-ionen (OH-).
Wanneer u H+ ionen toevoegt aan een neutrale oplossing:
* De concentratie van H+ ionen neemt toe.
* Dit verschuift de balans, waardoor de concentratie van H+ hoger is dan OH-.
* De pH van de oplossing neemt af en verplaatst deze naar het zure bereik.
Voorbeeld:
* Puur water is neutraal met een pH van 7.
* Het toevoegen van een zuur zoals zoutzuur (HCL) aan water geeft H+ ionen vrij.
* Dit verhoogt de H+ -concentratie, waardoor het waterzuur is (pH minder dan 7).
Samenvattend verhoogt het toevoegen van waterstofionen aan een neutrale oplossing de zuurgraad van de oplossing door de pH te verlagen.
 Warm oceaanwater vertraagt zee-ijs voor steden in Alaska, dieren in het wild
Warm oceaanwater vertraagt zee-ijs voor steden in Alaska, dieren in het wild Wetenschappers:soorten essen op de rand van uitsterven
Wetenschappers:soorten essen op de rand van uitsterven Holoceentemperatuur op het Iberisch schiereiland gereconstrueerd met subfossielen van insecten
Holoceentemperatuur op het Iberisch schiereiland gereconstrueerd met subfossielen van insecten Uitlaatgas is de schuldige:ozon op leefniveau is schadelijk voor gewassen
Uitlaatgas is de schuldige:ozon op leefniveau is schadelijk voor gewassen Big Muddy Missouri rivier heeft een plan nodig
Big Muddy Missouri rivier heeft een plan nodig
Hoofdlijnen
- Wat is een eigenschapsvariatie die verborgen is door de aanwezigheid van een andere variatie?
- Wat bepaalt wat er in en uit de cel beweegt?
- Wat wetenschapscommunicatoren zouden kunnen leren van marketingprofessionals
- Wat is de wetenschappelijke naam of taxonomische classificatie van giftige planten Clivia?
- Vooruitgang in de genomica van populieren:vrijwel naadloze genoomassemblage onthult nieuwe inzichten en toepassingen
- Wat zijn kenmerken van het leven die aangetoond zijn in cellulaire ademhaling?
- Nieuwe studie werpt licht op hoe de vroegste vormen van leven op aarde zijn geëvolueerd
- Resultaten van Landmark NASA DNA Twin Study zijn binnen
- Wat zijn 3 functies van DNA?
- Wetenschappers ontwikkelen sondes om acuut nierfalen vroegtijdig te detecteren
- Een filament dat geschikt is voor de ruimte - het is bewezen dat zijde gedijt bij temperaturen in de ruimte

- Strontium-iridiumoxide gebruikt voor maatwerk als elektronisch materiaal

- Haarverf is giftig - kunnen natuurlijke alternatieven worden gemaakt om te werken?

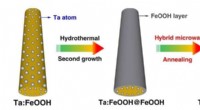
- Een stap dichter bij praktische zonne-waterstofproductie via uitgebreid gemodificeerde hematiet-fotoanode
 Wat is de oorzaak van gloeiende kleuren in poolatmosferen?
Wat is de oorzaak van gloeiende kleuren in poolatmosferen?  Kan ioniserende straling intern of extern worden gegeven?
Kan ioniserende straling intern of extern worden gegeven?  Voorbeeld van homogeen mengsel en heterogeen mengsel?
Voorbeeld van homogeen mengsel en heterogeen mengsel?  Geweld door hittegolf, Groenland ziet enorme ijssmelting
Geweld door hittegolf, Groenland ziet enorme ijssmelting Een molecuul ammoniak bestaat uit één atoomstikstof en drie atomen waterstof is NH3 een element of een verbinding?
Een molecuul ammoniak bestaat uit één atoomstikstof en drie atomen waterstof is NH3 een element of een verbinding?  Retinacellen gekweekt op nanovezelsteigers kunnen blindheid helpen behandelen
Retinacellen gekweekt op nanovezelsteigers kunnen blindheid helpen behandelen  Nieuwe theorie belooft de manier waarop we denken over polymeersuperstructuren te hervormen
Nieuwe theorie belooft de manier waarop we denken over polymeersuperstructuren te hervormen  Wat is het verschil tussen covalente en ionische bindingen?
Wat is het verschil tussen covalente en ionische bindingen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

