
Wetenschap
Hoe vind je de molaire massa van een verbinding met behulp van een periodieke tabel?
1. Identificeer de elementen en hun subscripten
* Kijk naar de chemische formule van de verbinding. Laten we bijvoorbeeld eens kijken naar water (h₂o).
* U hebt waterstof (H) en zuurstof (O).
* Het subscript "2" na waterstof betekent dat er twee waterstofatomen zijn in elk watermolecuul.
2. Zoek atomaire massa's op op het periodiek systeem
* Zoek elk element op het periodieke tabel.
* Let op de atomaire massa van elk element. Atomische massa's worden meestal getoond onder het symbool van het element. Bijvoorbeeld:
* Waterstof (h):1,01 g/mol
* Zuurstof (O):16,00 g/mol
3. Vermenigvuldig atoommassa met subscript
* Vermenigvuldig voor elk element zijn atomaire massa met zijn subscript in de chemische formule.
* Waterstof (h):1,01 g/mol * 2 =2,02 g/mol
* Zuurstof (O):16.00 g/mol * 1 =16.00 g/mol
4. Voeg de massa bij elkaar toe
* Voeg de resultaten van stap 3 toe om de molaire massa van de verbinding te vinden.
* Molaire watermassa (H₂o):2,02 g/mol + 16,00 g/mol =18,02 g/mol
Voorbeeld:het vinden van de molaire massa calciumchloride (CaCl₂)
1. Elementen:calcium (Ca) en chloor (CL)
2. Atomische massa's:
* Calcium (CA):40,08 g/mol
* Chloor (CL):35,45 g/mol
3. Vermenigvuldigde massa's:
* Calcium (CA):40,08 g/mol * 1 =40,08 g/mol
* Chloor (CL):35,45 g/mol * 2 =70,90 g/mol
4. Molaire massa:40,08 g/mol + 70,90 g/mol =110,98 g/mol
Sleutelpunten:
* eenheden: Molaire massa wordt tot expressie gebracht in gram per mol (g/mol).
* Significante cijfers: Let op het aantal belangrijke cijfers in de atoommassa's die u gebruikt. Rond uw laatste antwoord op de juiste manier af.
* Oefening: Hoe meer je oefent, hoe gemakkelijker het wordt om molaire massa te berekenen.
 Wat is de moleculaire formule voor Eicosane met 20 koolstofatomen?
Wat is de moleculaire formule voor Eicosane met 20 koolstofatomen?  De toestandsverandering van een vaste stof rechtstreeks naar een gas zonder de vloeibare toestand te passeren?
De toestandsverandering van een vaste stof rechtstreeks naar een gas zonder de vloeibare toestand te passeren?  Is staal een elementverbinding, pure stof of mengsel?
Is staal een elementverbinding, pure stof of mengsel?  Wat is functionele complementatie?
Wat is functionele complementatie?  Elektrodeontwerp maakt de weg vrij voor betere biobrandstofcellen, elektrochemische apparaten
Elektrodeontwerp maakt de weg vrij voor betere biobrandstofcellen, elektrochemische apparaten
 Wetsvoorstel om weersvoorspellingen te verbeteren gaat naar presidentsbureau
Wetsvoorstel om weersvoorspellingen te verbeteren gaat naar presidentsbureau Onderzoek vindt dramatische toename van overstromingen op kustwegen
Onderzoek vindt dramatische toename van overstromingen op kustwegen Internationaal onderzoeksteam roept op tot glokale aanpak om schade door overstromingen te helpen beperken
Internationaal onderzoeksteam roept op tot glokale aanpak om schade door overstromingen te helpen beperken Uw kraanwater kan plastic, onderzoekers waarschuwen (Update)
Uw kraanwater kan plastic, onderzoekers waarschuwen (Update) Typen heterotrofe bacteriën
Typen heterotrofe bacteriën
Hoofdlijnen
- Een 'aardbeving' in de cel:wetenschappers ontdekken hoe een wijziging van de nucleaire lamina zijn vorm behoudt
- Welke organel wordt gevonden in plantencellen en geen dierlijke cellen?
- Rechtbank vindt het goed om een soort uil te doden om het effect op andere uilen te zien
- Hoe zijn 2 organismen dezelfde soort?
- Onderzoek onthult een meesterregulator die schimmelinfectie van tarwe controleert
- Wat zijn attributen van een goede hypothese?
- Wilde paarden in het hoge land van Australië beschadigen veengebieden, waardoor de koolstofvoorraden afnemen
- Wat calla carnivore dat zijn eigen eten doodt?
- Wat identificeert een X- en Y -chromosoom?
- Wetenschappers creëren een kristal in een kristal voor nieuwe elektronische apparaten

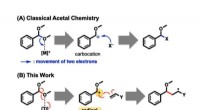
- Radicale chemie maakt eenvoudige synthese van ethers mogelijk
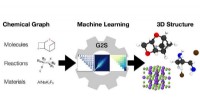
- Van chemische grafieken tot structuren
- Een bondgenoot voor legeringen:AI helpt bij het ontwerpen van hoogwaardig staal

- Nieuw onderzoek heeft tot doel de pijnstillende geheimen van dodelijk slakkengif te ontrafelen

 Het bereiken van 90% PL-kwantumopbrengst in 1-D metaalhalogenide door drukonderdrukt niet-stralingsverlies
Het bereiken van 90% PL-kwantumopbrengst in 1-D metaalhalogenide door drukonderdrukt niet-stralingsverlies Ontdekking van een lichtgevend sterrenstelsel dat 13 miljard jaar geleden het lokale intergalactische medium opnieuw ioniseert
Ontdekking van een lichtgevend sterrenstelsel dat 13 miljard jaar geleden het lokale intergalactische medium opnieuw ioniseert De spil van Facebook gaat minder over privacy en meer over winst
De spil van Facebook gaat minder over privacy en meer over winst Paden in welke objecten reizen rond de zon?
Paden in welke objecten reizen rond de zon?  Studie vindt dat ethiek kan worden onderwezen - in financiën, minstens
Studie vindt dat ethiek kan worden onderwezen - in financiën, minstens Wat zijn de namen van fasen maan en wanneer komen ze voor?
Wat zijn de namen van fasen maan en wanneer komen ze voor?  Onderzoeksteam ontwikkelt een krachtige quantum-dot-modus-vergrendelde laser op silicium
Onderzoeksteam ontwikkelt een krachtige quantum-dot-modus-vergrendelde laser op silicium Waarom menselijke cellen identiek?
Waarom menselijke cellen identiek?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

