
Wetenschap
Waarom doen atomen zich aan bij een chemische binding?
Hier is een uitsplitsing van hoe dit werkt:
* elektronen en stabiliteit: Atomen zijn het meest stabiel wanneer hun buitenste elektronenschil (valentieschaal) vol is. Dit wordt meestal bereikt door 8 elektronen te hebben (de "octetregel").
* delen of overbrengen: Om een volledige valentie -schaal te bereiken, kunnen atomen elektronen delen met andere atomen (covalente binding) of elektronen volledig overbrengen naar een ander atoom (ionische binding).
* Lagere energietoestand: Het proces van het vormen van chemische bindingen brengt energie vrij, waardoor de atomen naar een lagere energietoestand worden verplaatst, wat stabieler is.
Hier is een vereenvoudigde analogie:
Stel je voor dat elk atoom een persoon is die zich compleet en gelukkig wil voelen. Ze hebben "zakken" (valentieschalen) die moeten worden gevuld met 8 "knikkers" (elektronen). Door knikkers te delen of te geven, kunnen ze zowel een volledige set bereiken als inhoud voelen, waardoor een binding (vriendschap) tussen hen wordt gecreëerd.
Hier zijn enkele andere factoren die de vorming van de binding beïnvloeden:
* Elektrostatische aantrekkingskracht: De positieve kern van het ene atoom wordt aangetrokken door de negatieve elektronen van een ander atoom. Deze kracht helpt atomen bij elkaar te houden.
* elektronegativiteit: De neiging van een atoom om elektronen in een binding aan te trekken. Verschillende elektronegativiteiten leiden tot verschillende soorten bindingen (polaire covalente, niet -polaire covalente, ionische).
Samenvattend: Atomen vormen chemische bindingen om een stabielere toestand te bereiken door hun buitenste elektronenschil te vullen, die uiteindelijk hun energie verlaagt. Dit proces wordt aangedreven door elektrostatische aantrekkingskracht en beïnvloed door factoren zoals elektronegativiteit.
 Hoe is het gebruik van wetenschap gerelateerd aan de context in de samenleving?
Hoe is het gebruik van wetenschap gerelateerd aan de context in de samenleving?  Californië kan de grote vervuilers niet laten winnen door de wetten inzake openbaarmaking van klimaatverandering te ondermijnen
Californië kan de grote vervuilers niet laten winnen door de wetten inzake openbaarmaking van klimaatverandering te ondermijnen  Tropische droge bosplanten
Tropische droge bosplanten Lokaal en plantaardig eten:hoe steden duurzaam te voeden?
Lokaal en plantaardig eten:hoe steden duurzaam te voeden? Hier is methaan:wetenschappers onderzoeken de oorsprong van een gapende permafrostkrater
Hier is methaan:wetenschappers onderzoeken de oorsprong van een gapende permafrostkrater
Hoofdlijnen
- Welke celorganel combineert met een blaasje voor de digestie?
- Het redden van de Mary River-schildpad:hoe de mensen van Tiaro zich achter een iconische soort schaarden
- Wilde kapucijnapen met baard weten echt hoe ze een noot moeten kraken
- Hoe belemmert de wetenschap geneeskunde?
- Waarom is een blad een orgel?
- Wat zijn de functies van enzymen?
- Studie:Het evolutionaire verleden kan bepalen hoe we leiders kiezen
- Wat is de naam van een complex individu dat orgaansystemen bestaat?
- Waarom is een pH-waarde van 7,8 het beste om de enzymactiviteit te beïnvloeden?
- Hydrogel-composiet ontwikkeld om beschermende uitrusting te helpen snel giftige zenuwgassen af te breken

- Eenvoudige en kosteneffectieve winning van zeldzame metalen uit industrieel afval

- Chemicus creëert katalysator om anti-muggenstoffen te produceren
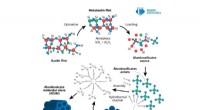
- De multitasking-katalysator

- Studie onthult kenmerken van SARS-CoV-2 spike-eiwit

 Het AI-model vergelijkt rechtstreeks de eigenschappen van potentiële nieuwe medicijnen
Het AI-model vergelijkt rechtstreeks de eigenschappen van potentiële nieuwe medicijnen  Berekening van steekproefgrootte Formula
Berekening van steekproefgrootte Formula De droogste plek op aarde:de Chileense Atacama-woestijn
De droogste plek op aarde:de Chileense Atacama-woestijn  NASA ziet tropische storm Bebinca nog steeds nabij het eiland Hainan
NASA ziet tropische storm Bebinca nog steeds nabij het eiland Hainan Hoe ontstaan silicaatmineralen?
Hoe ontstaan silicaatmineralen?  Eiwit ontdekt in meteoriet
Eiwit ontdekt in meteoriet Welke informatie kan niet worden verkregen uit het Human Genome Project?
Welke informatie kan niet worden verkregen uit het Human Genome Project?  Studie gebruikt een elektrisch veld om magnetische eigenschappen te creëren in niet-magnetisch materiaal
Studie gebruikt een elektrisch veld om magnetische eigenschappen te creëren in niet-magnetisch materiaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

