
Wetenschap
Hoeveel mol SO3 zou worden geproduceerd wanneer 1,2 zuurstof wordt geconsumeerd in de vergelijking S plus O2 is gelijk aan SO3?
Hier is hoe dit probleem op te lossen:
1. Evenwichtige chemische vergelijking:
Ten eerste moeten we de chemische vergelijking in evenwicht brengen:
S + 1,5 o₂ → So₃
2. Mol -verhouding:
Uit de evenwichtige vergelijking zien we dat 1,5 mol O₂ reageert om 1 mol SO₃ te produceren.
3. Berekening:
Omdat u 1,2 mol O₂ hebt geconsumeerd, kunnen we een deel instellen:
(1 mol SO₃ / 1,5 mol O₂) =(x mol So₃ / 1.2 mol o₂)
Oplossen voor X:
x mol so₃ =(1 mol So₃ / 1,5 mol o₂) * (1,2 mol o₂) = 0,8 mol So₃
Daarom zou 0,8 mol SO₃ worden geproduceerd wanneer 1,2 mol zuurstof wordt geconsumeerd.
 Een nieuw op polyethyleen-B4C gebaseerd beton voor afscherming
Een nieuw op polyethyleen-B4C gebaseerd beton voor afscherming Wat is de molaire oplosbaarheid van PBBR2 in water?
Wat is de molaire oplosbaarheid van PBBR2 in water?  Definitie van representatief element
Definitie van representatief element  Wat zou er gebeuren met de oplosbaarheid van een gas in water als het volume zou worden verminderd maar constant bleef?
Wat zou er gebeuren met de oplosbaarheid van een gas in water als het volume zou worden verminderd maar constant bleef?  Waarom heeft zwavel zijn naam?
Waarom heeft zwavel zijn naam?
Hoofdlijnen
- Wat zijn enkele wetenschappelijke carrières?
- Hoe komt de zebravis aan zijn strepen? Onderzoekers zijn een stap dichter bij het vinden ervan
- Hebben aardappelen meer chromosomen dan mensen?
- Hoe een schadelijke schimmel zijn waardplant weerloos maakt
- Kunnen windturbines en trekvogels naast elkaar bestaan?
- Wat zijn het vrouwelijke orgaan van plantengedeelte dat eiercellen produceert?
- Zijn er meer eencellige of meercellige organismen op aarde?
- Elk menselijk gen is gesequenced als gevolg van wat?
- Een nieuw begrip van hoe COVID mensen infecteert
- Biodiesel maken van vuile oude frituurolie is nu een stuk eenvoudiger geworden

- Een nieuwe methode voor proximity-labeling op nanometerschaal die zich richt op histidine-residuen

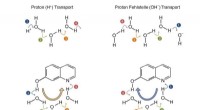
- Vooruit of achteruit? Nieuwe routes voor protonen in water of methanol
- Op zijde gebaseerde apparaten met antisense-miRNA-therapeutica kunnen de botregeneratie verbeteren

- Computationeel onderzoek beschrijft het activeringsmechanisme van p38-alpha

 Onderzoek toont aan hoe elektriciteitetende microben elektronen gebruiken om koolstofdioxide vast te leggen
Onderzoek toont aan hoe elektriciteitetende microben elektronen gebruiken om koolstofdioxide vast te leggen  Arctische vergroening ontdooit permafrost, verhoogt de afvoer
Arctische vergroening ontdooit permafrost, verhoogt de afvoer Hoe ionen watermoleculen om zich heen verzamelen
Hoe ionen watermoleculen om zich heen verzamelen  Zijn er risico’s verbonden aan de productie van windenergie?
Zijn er risico’s verbonden aan de productie van windenergie?  Hoe de zijlengten van driehoeken te vinden
Hoe de zijlengten van driehoeken te vinden  Nieuwe megabibliotheekbenadering blijkt nuttig voor de snelle ontdekking van nieuwe materialen
Nieuwe megabibliotheekbenadering blijkt nuttig voor de snelle ontdekking van nieuwe materialen Pathfinder-satelliet maakt de weg vrij voor constellatie van waarnemers van tropische stormen
Pathfinder-satelliet maakt de weg vrij voor constellatie van waarnemers van tropische stormen Hoe de beperkende reactie te vinden in Stoichiometry
Hoe de beperkende reactie te vinden in Stoichiometry
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

