
Wetenschap
Wat is de oxidatietoestand van een individueel fosforatoom in PO4-3?
Hier leest u hoe u de oxidatietoestand van fosfor in Po₄⁻³ kunt bepalen:
1. Wijs oxidatietoestanden toe aan zuurstof
* Zuurstof heeft meestal een oxidatietoestand van -2.
* Omdat er vier zuurstofatomen zijn, is hun totale bijdrage -8.
2. Overweeg de algehele lading
* Het fosfaation (po₄⁻³) heeft een lading van -3.
3. Oplossen voor fosforus
* Laat 'x' de oxidatietoestand van fosfor vertegenwoordigen.
* De som van de oxidatietoestanden moet gelijk zijn aan de totale lading:
x + (-8) =-3
4. Bereken de oxidatietoestand van fosforus
* Los op voor 'x':
x =-3 + 8
x =+5
Daarom is de oxidatietoestand van een individueel fosforatoom in po₄⁻³ +5.
 Baanbrekende studie geeft nieuw inzicht in vorming van koperafzettingen
Baanbrekende studie geeft nieuw inzicht in vorming van koperafzettingen Earth-monitoring Landsat 9-satelliet gelanceerd in Californië
Earth-monitoring Landsat 9-satelliet gelanceerd in Californië NASA ziet tropische storm Man-yi naderen tyfoonsterkte Tropical Storm Man-Yi con
NASA ziet tropische storm Man-yi naderen tyfoonsterkte Tropical Storm Man-Yi con Wat geeft de aarde zijn ware vorm?
Wat geeft de aarde zijn ware vorm?  Waarom onderwijs in ondernemerschap mislukt in verarmde regio’s
Waarom onderwijs in ondernemerschap mislukt in verarmde regio’s
Hoofdlijnen
- Wat betekent conclusie en discussie in een wetenschap?
- Wat is lachyoga?
- Genetici lossen een veertig jaar oud dilemma op om te verklaren waarom dubbele genen in het genoom achterblijven
- Waarom zou een wetenschapper een analogie in rapport kunnen gebruiken?
- Wat zijn de mechanismen achter de verdrijving van zoöxanthella uit koraal?
- Zeldzame zangvogel heeft misschien nooit bestaan
- Wat veroorzaakt gisting?
- Welke macromoleculen worden gevonden in garnalen?
- Wat is het diafragma van op een microscoopcontrole?
- Hoogwaardige katalysatoren met één atoom voor brandstofcellen bij hoge temperaturen

- Silicium met een tweedimensionale structuur
- Wetenschappers ontwikkelen een manier om afvalplastic te gebruiken om autobrandstof te maken

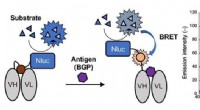
- Nieuw licht werpen:een nieuw type immunosensor voor immunoassaytests
- Een unieke katalysator maakt de weg vrij voor plastic upcycling
 Zou een waterige oplossing van ammoniumcarbonaat ionen bevatten?
Zou een waterige oplossing van ammoniumcarbonaat ionen bevatten?  Welke rots wordt gevormd uit zand en zout?
Welke rots wordt gevormd uit zand en zout?  Ammonium? - Antwoorden
Ammonium? - Antwoorden  Welke apparaten kan ik gebruiken met een stroomgenerator van 6500 watt?
Welke apparaten kan ik gebruiken met een stroomgenerator van 6500 watt?  De vorm van een combinatie twee eigenschappen die verborgen kunnen worden, wordt eigenschap genoemd?
De vorm van een combinatie twee eigenschappen die verborgen kunnen worden, wordt eigenschap genoemd?  Kan Twitter rampenbestrijding ondersteunen? Nieuw onderzoek onderzoekt hoe
Kan Twitter rampenbestrijding ondersteunen? Nieuw onderzoek onderzoekt hoe  NASA vindt tropische cycloon Wutip aan het organiseren
NASA vindt tropische cycloon Wutip aan het organiseren TESS heeft duizenden mogelijke exoplaneten gevonden:welke moet JWST bestuderen?
TESS heeft duizenden mogelijke exoplaneten gevonden:welke moet JWST bestuderen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

