
Wetenschap
Wat veroorzaakt de pH van een oplossing?
1. Toevoeging van een basis:
* Bases zijn stoffen die hydroxide-ionen (OH-) doneren wanneer ze in water worden opgelost.
* Voorbeelden zijn:
* Sterke bases: Natriumhydroxide (NaOH), kaliumhydroxide (KOH)
* Zwakke bases: Ammoniak (NH3), bakpoeder (natriumbicarbonaat, NAHCO3)
* Wanneer u een basis aan een oplossing toevoegt, verhoogt dit direct de concentratie van OH-, wat leidt tot een hogere pH.
2. Verwijdering van waterstofionen:
* Het verwijderen van H+ -ionen uit een oplossing verschuift ook de balans naar een hogere pH. Dit kan gebeuren door:
* reactie met een basis: Zuren reageren met basen om elkaar te neutraliseren, H+ te consumeren en water te genereren.
* reactie met een metaal: Sommige metalen reageren met zuren om zouten te vormen en waterstofgas vrij te geven (H2).
3. Temperatuurveranderingen:
* Temperatuur beïnvloedt de ionisatie van water: Bij hogere temperaturen hebben watermoleculen vaker ionen, waardoor meer H+ en OH- produceren. De toename van OH- is echter over het algemeen groter, wat leidt tot een lichte toename van de pH.
4. Bepaalde zouten oplossen:
* Sommige zouten, wanneer opgelost in water, kunnen hydrolyseren, wat betekent dat ze met water reageren om H+ of OH- te produceren.
* zouten van zwakke zuren en sterke basen: Deze zouten hebben de neiging om te hydrolyseren om OH- te produceren, waardoor de pH wordt verhoogd. Voorbeeld:natriumacetaat (CH3Coona).
* zouten van sterke zuren en zwakke basen: Deze zouten hebben de neiging om te hydrolyseren om H+te produceren, waardoor de pH wordt verlaagd. Voorbeeld:ammoniumchloride (NH4CL).
Belangrijke opmerking:
* pH is een logaritmische schaal. Een verandering van één pH-eenheid vertegenwoordigt een tienvoudige verandering in de concentratie van H+ of OH-.
* De pH van een oplossing is een maat voor de zuurgraad of alkaliteit. Een pH onder de 7 is zuur, een pH van 7 is neutraal en een pH boven 7 is alkalisch (basic).
 Wat gebeurt er als je vier verschillende pepermuntjes in vloeistoffen doet?
Wat gebeurt er als je vier verschillende pepermuntjes in vloeistoffen doet?  Mendeleev rangschikt de bekende chemische elementen in een tabel volgens incassering?
Mendeleev rangschikt de bekende chemische elementen in een tabel volgens incassering?  Wat is de covalente verbinding van NO2?
Wat is de covalente verbinding van NO2?  Wat gebeurt er met een gemengde calciumchlorideoplossing en natriumcarbonaatfiltratie? Was het residu met gedestilleerd water, laat het drogen en voeg zoutzuur toe?
Wat gebeurt er met een gemengde calciumchlorideoplossing en natriumcarbonaatfiltratie? Was het residu met gedestilleerd water, laat het drogen en voeg zoutzuur toe?  Lichaam Hoe doneren aan de wetenschap werkt
Lichaam Hoe doneren aan de wetenschap werkt
 Telecom zendmasten kunnen worden gebruikt om regen te voorspellen
Telecom zendmasten kunnen worden gebruikt om regen te voorspellen Wat is de betekenis van abstract in het onderzoeksproject?
Wat is de betekenis van abstract in het onderzoeksproject?  Conspiracisme toont aan hoe belangrijk het is om te onderzoeken hoe bewijsmateriaal wordt gebruikt
Conspiracisme toont aan hoe belangrijk het is om te onderzoeken hoe bewijsmateriaal wordt gebruikt  Voedingscomponenten verminderen de biologische beschikbaarheid van cadmium in rijst
Voedingscomponenten verminderen de biologische beschikbaarheid van cadmium in rijst Fijnstof vergroot droogte kwetsbaarheid bomen
Fijnstof vergroot droogte kwetsbaarheid bomen
Hoofdlijnen
- Welke reactie produceert sucrose uit glucose en fructose?
- Drie hoofdafdelingen van de hersenen?
- Wanneer wetenschappers hun vijf zintuigen gebruiken, verzamelt dit wat voor soort informatie?
- Onderzoekers ontdekken details over hoe bacteriën beschermende barrières bouwen, wat nieuwe antibiotica kan opleveren
- Waar in de cel bevinden zich enzymen?
- Welke structuur maakt bloedcellen en zorgen voor spieren om te hechten?
- Wat zijn aanstootgevende micro -organismen?
- Wat zijn de namen van cellen in STEM?
- Wat zijn de voorbeelden van ziekten in planten?
- Nieuwe schaal voor elektronegativiteit herschrijft het leerboek scheikunde

- Chemisch ingenieur ontwikkelt styreenvrije bio-hernieuwbare harsen

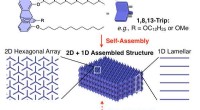
- Zelfassemblerende polymeren op siliconenbasis
- Video:vijf dingen die je misschien niet wilt combineren met anticonceptie

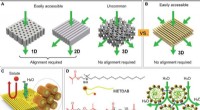
- Zelf-geassembleerd membraan met water-continue transportroutes voor nauwkeurige nanofiltratie
 SpaceX boekt zijn eerste privépassagier naar de maan
SpaceX boekt zijn eerste privépassagier naar de maan  SpaceXs opgewaardeerde raket vliegt met satelliet voor Bangladesh
SpaceXs opgewaardeerde raket vliegt met satelliet voor Bangladesh Sprint verhoogt mobiele hotspot naar 50GB, schakelt sneller 4G LTE-netwerk in voordat 5G in 2019 arriveert
Sprint verhoogt mobiele hotspot naar 50GB, schakelt sneller 4G LTE-netwerk in voordat 5G in 2019 arriveert Google, EU brengt strijd voor de rechter
Google, EU brengt strijd voor de rechter Hoe u e-mailcommunicatie kunt verbeteren:Het ontwikkelen van strategieën bootst face-to-face interacties na
Hoe u e-mailcommunicatie kunt verbeteren:Het ontwikkelen van strategieën bootst face-to-face interacties na  Wat is de gezondste plant ter wereld?
Wat is de gezondste plant ter wereld?  Een Bubble Gum Science-project maken
Een Bubble Gum Science-project maken Laat je niet misleiden door mooi eten, onderzoek waarschuwt
Laat je niet misleiden door mooi eten, onderzoek waarschuwt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

