
Wetenschap
Welk volume zuurstofgas bij 320K en 680 TORR zal reageren met 2,50 L?
* De identiteit van de andere reactant: U moet weten waarmee het zuurstofgas reageert. Dit zal de stoichiometrie van de reactie bepalen.
* De druk en temperatuur van de andere reactant: Om het benodigde volume van zuurstof te berekenen, moet u de omstandigheden van de andere reactant kennen, zodat u het aantal betrokken mol kunt berekenen.
Hier is een voorbeeld van hoe u het probleem kunt oplossen zodra u die informatie hebt:
Voorbeeld:
Laten we zeggen dat het zuurstofgas reageert met 2,50 L waterstofgas bij 320 K en 680 TORR. De reactie is:
2 H₂ (G) + O₂ (G) → 2 H₂o (G)
1. Bereken mol waterstof:
* Gebruik de ideale gaswet:PV =NRT
* P =680 TORR =0.895 ATM (converteer Torr naar ATM)
* V =2,50 l
* R =0,0821 l ATM/MOL K
* T =320 K
* n =(pv) / (rt) =(0.895 atm * 2,50 l) / (0,0821 l atm / mol k * 320 k) =0,085 mol H₂
2. Bepaal de benodigde mol zuurstof:
* Uit de evenwichtige vergelijking reageren 2 mol H₂ met 1 mol o₂.
* Mol O₂ =(0,085 mol H₂) * (1 mol O₂ / 2 mol H₂) =0,0425 mol O₂
3. Bereken volume zuurstof:
* Gebruik opnieuw de ideale gaswet, oplossen voor volume (v):
* V =(nrt) / p
* n =0,0425 mol
* R =0,0821 l ATM/MOL K
* T =320 K
* P =680 TORR =0.895 ATM
* V =(0,0425 mol * 0,0821 l ATM/mol K * 320 K)/0.895 atm = 1,27 L o₂
Daarom zou 1,27 L zuurstofgas bij 320 K en 680 Torr nodig zijn om onder dezelfde omstandigheden te reageren met 2,50 L waterstofgas.
Onthoud: Dit is slechts een voorbeeld. U moet de berekeningen aanpassen op basis van de specifieke reactie en voorwaarden die in uw probleem worden gegeven.
 Doet alleen chemische reacties zich voor in levende organismen?
Doet alleen chemische reacties zich voor in levende organismen?  Waarom hebben planten water nodig in fotosynthese?
Waarom hebben planten water nodig in fotosynthese?  Gemakkelijk waarnemen van schadelijke stoffen die milieuvervuiling veroorzaken via de camera van een mobiele telefoon
Gemakkelijk waarnemen van schadelijke stoffen die milieuvervuiling veroorzaken via de camera van een mobiele telefoon  Hoe heb je geprobeerd het uit en weer aan te zetten? werkt voor de chemie, niet alleen voor computers
Hoe heb je geprobeerd het uit en weer aan te zetten? werkt voor de chemie, niet alleen voor computers  Hoe wordt het aantal elektronen in de buitenste schil genoemd?
Hoe wordt het aantal elektronen in de buitenste schil genoemd?
 Geo-engineering kan tropische veengronden destabiliseren
Geo-engineering kan tropische veengronden destabiliseren Vulkanisme zorgde voor snelle deoxygenatie van de oceaan in de tijd van de dinosauriërs
Vulkanisme zorgde voor snelle deoxygenatie van de oceaan in de tijd van de dinosauriërs Het volgende grote gevecht tussen Californië en Trump gaat over water en bedreigde diersoorten
Het volgende grote gevecht tussen Californië en Trump gaat over water en bedreigde diersoorten Wetenschappers doen ontdekking over stroming van kustwater
Wetenschappers doen ontdekking over stroming van kustwater Meeuwen:schildwachten van bacteriën in de omgeving
Meeuwen:schildwachten van bacteriën in de omgeving
Hoofdlijnen
- Hoe functioneert glycogeen in levende dingen?
- Welke soort is het meest geschikt voor het leven? Allen hebben een gelijke kans, wetenschappers zeggen:
- Bomen op een universiteitscampus doorstaan droogte dankzij lekkende leidingen
- Doodt ontvetter of desinfectiemiddel bacteriën?
- Reduceren, hergebruiken, reflycleeren:hoe genetisch gemodificeerde vliegen afval kunnen verminderen en uit de stortplaatsen kunnen houden
- Welk deel van een dierencel is vergelijkbaar met je huid?
- Wat wordt bedoeld met de stelling dat DNA alle organismen verenigt?
- Is het verschil tussen glycogeen en zetmeel?
- Wie heeft Botany opgericht?
- Nieuwe technologie maakt snelle eiwitsynthese mogelijk

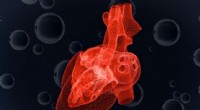
- Studie voorspelt reactie van hartcellen op afnemende zuurstof
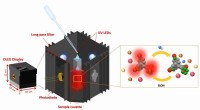
- Nieuw apparaat vereenvoudigt meting van fluorideverontreiniging in water
- Cyborg-technologie kan nieuwe diagnostiek mogelijk maken, samensmelting van mens en AI
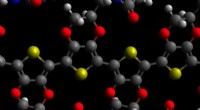
- Overgangsmetaalcomplexen:gemengd werkt beter

 Hoe wordt de samenstelling van een planeet bepaald?
Hoe wordt de samenstelling van een planeet bepaald?  Opruiming Fukushima vermindert stralingsniveaus, maar niet alles
Opruiming Fukushima vermindert stralingsniveaus, maar niet alles Hoe verschilt de representatieve eenheid van een moleculaire verbinding van een ionische verbinding?
Hoe verschilt de representatieve eenheid van een moleculaire verbinding van een ionische verbinding?  Hoe zal de aarde er over 5000 jaar uitzien?
Hoe zal de aarde er over 5000 jaar uitzien?  Wat gebeurt er met het aantal witte bloedcellen tijdens een infectie?
Wat gebeurt er met het aantal witte bloedcellen tijdens een infectie?  Hoe verhoudt Moon zich tot Ganymede?
Hoe verhoudt Moon zich tot Ganymede?  Expert bespreekt wat COVID-19 betekent voor immigratie
Expert bespreekt wat COVID-19 betekent voor immigratie Doorbraak in silicium kan de belangrijkste microgolftechnologie veel goedkoper en beter maken
Doorbraak in silicium kan de belangrijkste microgolftechnologie veel goedkoper en beter maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

