
Wetenschap
Wat is de waterstofperoxidefunctie?
1. Oxidatiemiddel:
* Antiseptisch en desinfectiemiddel: Dit is het meest voorkomende gebruik. Waterstofperoxide breekt af in water en zuurstofgas wanneer het in contact komt met organisch materiaal, zoals bacteriën, virussen en schimmels. Deze reactieve zuurstofspecies (ROS) kan microben doden door hun celmembranen te beschadigen en hun interne componenten te oxideren.
* bleekmiddel: Het kan haar en bleekstoffen verlichten door melanine en andere pigmenten af te breken.
* chemische synthese: Gebruikt bij de productie van verschillende chemicaliën, waaronder organische peroxiden, epoxiden en polymeren.
2. In biologische systemen:
* Cellulaire signalering: Waterstofperoxide werkt als een signaalmolecuul in levende cellen. Het kan verschillende cellulaire responsen veroorzaken, waaronder genexpressie en celgroei.
* Immuunrespons: Het immuunsysteem gebruikt waterstofperoxide om pathogenen te doden en infecties te bestrijden.
* Wondgenezing: Het is betrokken bij het genezingsproces door de vorming van nieuw weefsel te bevorderen.
3. Industriële toepassingen:
* Papier- en pulpindustrie: Gebruikt in bleekprocessen.
* Voedselindustrie: Gebruikt als een desinfectiemiddel en om voedsel te behouden.
* Waterbehandeling: Gebruikt om ijzer en mangaan uit water te verwijderen.
belangrijke opmerkingen:
* concentratie is belangrijk: De concentratie van waterstofperoxide bepaalt de effectiviteit en veiligheid ervan. Verdunde oplossingen zijn over het algemeen veilig voor actueel gebruik, maar geconcentreerd waterstofperoxide kan gevaarlijk zijn en mogen alleen worden gebruikt met de juiste voorzorgsmaatregelen.
* veiligheidsproblemen: Hoge concentraties waterstofperoxide kunnen huidirritatie, brandwonden en zelfs blindheid veroorzaken als het in de ogen komt. Het moet met zorg worden behandeld.
Samenvattend is waterstofperoxide een veelzijdige verbinding met een reeks functies, van desinfecterende wonden tot het bleken van stoffen. Het is echter belangrijk om de eigenschappen ervan te begrijpen en veilig te gebruiken.
 Een verandering is de volgorde van aminozuren?
Een verandering is de volgorde van aminozuren?  Een antibioticum dat zich voordoet als een natuurlijke verbinding in de gigantische Madeiraanse squill
Een antibioticum dat zich voordoet als een natuurlijke verbinding in de gigantische Madeiraanse squill Nieuwe milieuvriendelijke vleesanaloog gezonder, biedt meer smaken
Nieuwe milieuvriendelijke vleesanaloog gezonder, biedt meer smaken Wat is het aminozuur dat verantwoordelijk is voor de reactie van Hopkins-Cole?
Wat is het aminozuur dat verantwoordelijk is voor de reactie van Hopkins-Cole?  Onderzoekers ontwikkelen duurzame wondverbandhydrogel op basis van zeewier en koolzuurhoudend water
Onderzoekers ontwikkelen duurzame wondverbandhydrogel op basis van zeewier en koolzuurhoudend water
 Krill zou een geheim wapen kunnen zijn in de strijd tegen plastic in de oceaan
Krill zou een geheim wapen kunnen zijn in de strijd tegen plastic in de oceaan Wat gebeurt er met luchtdruk als u zich verplaatst van de troposfeer naar de thermosfeer?
Wat gebeurt er met luchtdruk als u zich verplaatst van de troposfeer naar de thermosfeer?  Hebben onderzoekers de ontbrekende schakel gevonden die het mysterieuze fenomeen verklaart dat bekend staat als sprookjescirkels?
Hebben onderzoekers de ontbrekende schakel gevonden die het mysterieuze fenomeen verklaart dat bekend staat als sprookjescirkels?  Hoe vuur van vandaag het water van morgen zal beïnvloeden
Hoe vuur van vandaag het water van morgen zal beïnvloeden Seismisch forensisch onderzoek en het belang ervan voor vroegtijdige waarschuwing
Seismisch forensisch onderzoek en het belang ervan voor vroegtijdige waarschuwing
Hoofdlijnen
- Wat is een voorbeeld van intern en extern in wetenschapsdefinities?
- Hoe weet het lichaam hoe hij mRNA moet produceren?
- Nieuwe theorie daagt de huidige kijk uit op hoe de hersenen langetermijngeheugen opslaan
- Cephalization of Earthworms
- Wat je studeert en waar doet er toe, maar dat geldt ook voor het inkomen van je ouders
- Wetenschappers ontwikkelen nieuwe techniek om het verborgen genoom te onthullen
- Wat is een voorbeeld van hoe wetenschapper gegevens verzamelen?
- Bij welk type symbiose leven bacteriën in de darmen van een koe om cellulose te helpen afbreken?
- Wat is de gelei-achtige stof in planten- en dierlijke cellen?
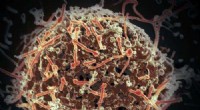
- Muterend Ebolas-sleuteleiwit kan replicatie stoppen
- Chemici banen een nieuwe weg in de zoektocht naar antibiotica

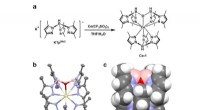
- Diepblauwe organische lichtemitterende diodes op basis van een doublet-emissie cerium(III)-complex
- Metaalhout naar nieuwe hoogten laten groeien

- Nieuwe microfluïdische chip verhoogt de gevoeligheid van immunoassays met 1000x

 Een maat voor hoe een vaste stof verlengt wanneer het wordt verwarmd?
Een maat voor hoe een vaste stof verlengt wanneer het wordt verwarmd?  Waarom voelen tienermeisjes zich aangetrokken tot jongens die hen pijn doen? We spraken met middelbare scholieren om erachter te komen
Waarom voelen tienermeisjes zich aangetrokken tot jongens die hen pijn doen? We spraken met middelbare scholieren om erachter te komen  Welke planeet in het zonnestelsel wordt elegante planeet genoemd?
Welke planeet in het zonnestelsel wordt elegante planeet genoemd?  De verbranding van kolen moet aan banden worden gelegd als de opwarming van de aarde deze eeuw tot 1,5 C moet worden beperkt
De verbranding van kolen moet aan banden worden gelegd als de opwarming van de aarde deze eeuw tot 1,5 C moet worden beperkt Wetenschappers ontdekken hoe mysterieus 'circulair RNA' wordt gevormd, claimen een verband met spierdystrofie
Wetenschappers ontdekken hoe mysterieus 'circulair RNA' wordt gevormd, claimen een verband met spierdystrofie  Uber, Postmates klagen aan om de nieuwe arbeidswet van Californië aan te vechten
Uber, Postmates klagen aan om de nieuwe arbeidswet van Californië aan te vechten Koolstofnanobuisjes zetten elektrische stroom om in quasi-deeltjes van lichte materie
Koolstofnanobuisjes zetten elektrische stroom om in quasi-deeltjes van lichte materie Zou de dichtheid zinken of vloeren water?
Zou de dichtheid zinken of vloeren water?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

