
Wetenschap
Waarom is de regulatie van de concentratie waterstofionen zo belangrijk?
1. Enzymactiviteit: Enzymen, de biologische katalysatoren die alle metabole reacties aandrijven, zijn zeer gevoelig voor pH. Elk enzym heeft een optimaal pH -bereik waar het het meest efficiënt functioneert. Een pH -verschuiving buiten dit bereik kan:
* Verminder enzymactiviteit: Het enzym bindt zijn substraat mogelijk niet correct of ondergaat conformationele veranderingen die zijn katalytische functie beïnvloeden.
* Denature Enzymen: Extreme pH -veranderingen kunnen de zwakke bindingen doorbreken die de structuur van het enzym bij elkaar houden, waardoor het inactief wordt.
2. Cellulaire processen: Veel essentiële cellulaire processen zijn pH-afhankelijk, waaronder:
* Cellulaire ademhaling: De productie van energie (ATP) door glycolyse en de Krebs -cyclus wordt strak geregeld door pH.
* eiwitsynthese: De assemblage van eiwitten uit aminozuren is gevoelig voor pH -veranderingen.
* Signaaltransductie: Veranderingen in pH kunnen werken als signalen in cellen, waardoor verschillende reacties worden geactiveerd.
* Membraanpermeabiliteit: De pH -gradiënt over celmembranen is van cruciaal belang voor het handhaven van celintegriteit en transportprocessen.
3. Bloed- en lichaamsvloeistofhomeostase:
* Bloed pH: Het handhaven van een stabiele pH van het bloed (rond 7,35-7,45) is essentieel voor zuurstoftransport door hemoglobine, de juiste zenuw- en spierfunctie en de algehele gezondheid van het orgaan.
* Andere lichaamsvloeistoffen: PH -onevenwichtigheden in andere vloeistoffen zoals cerebrospinale vloeistof of urine kunnen leiden tot verschillende fysiologische problemen.
4. Buffersystemen: Het lichaam heeft geavanceerde buffersystemen (zoals het bicarbonaatbuffersysteem in bloed) die onvermoeibaar werken om veranderingen in pH te weerstaan. Deze buffers minimaliseren de impact van zuren en basen die het lichaam voortdurend binnenkomen via metabole processen en externe bronnen.
5. Gevolgen van pH -onevenwichtigheden:
* acidose (lage pH): Kan leiden tot vermoeidheid, verwarring, ademhalingsmoeilijkheden en in ernstige gevallen, coma.
* alkalose (hoge pH): Kan spierkrampen, tintelingen en hyperventilatie veroorzaken.
Samenvattend is de regulatie van waterstofionconcentratie van vitaal belang voor het handhaven van de delicate balans die nodig is voor het leven. Juiste pH-regeling zorgt voor een optimale functie van enzymen, cellulaire processen en lichaamsvloeistoffen, wat bijdraagt aan de algehele gezondheid en welzijn.
 Hoe zijn frankium en lithium gerelateerd als 87 elektronen drie zijn?
Hoe zijn frankium en lithium gerelateerd als 87 elektronen drie zijn?  Hoe kan de massa van een atoom van periodiek worden weergegeven met betrekking tot mol?
Hoe kan de massa van een atoom van periodiek worden weergegeven met betrekking tot mol?  Onderzoekers streven naar goedkope, efficiënte technologieën voor waterstofopwekking
Onderzoekers streven naar goedkope, efficiënte technologieën voor waterstofopwekking Hoe veranderen neonlichten van kleur?
Hoe veranderen neonlichten van kleur?  Hoe rubberbanden smelten
Hoe rubberbanden smelten
 Kan het eten van insecten het wereldvoedseltekort oplossen?
Kan het eten van insecten het wereldvoedseltekort oplossen?  Pandemische afsluitingen resulteerden in minder smelten van sneeuw en ijs in het stroomgebied van de Indus
Pandemische afsluitingen resulteerden in minder smelten van sneeuw en ijs in het stroomgebied van de Indus Waterveiligheidscontroles onderschatten gevaarlijk de ziekteverwekkerniveaus, studie suggereert:
Waterveiligheidscontroles onderschatten gevaarlijk de ziekteverwekkerniveaus, studie suggereert: Bezitten oude steden de sleutel tot gelijke, duurzame stedelijke toegang?
Bezitten oude steden de sleutel tot gelijke, duurzame stedelijke toegang?  De Argentijnse strijd tegen megamining
De Argentijnse strijd tegen megamining
Hoofdlijnen
- Welke fysiologische aanpassing zou het transportproces in een plant verminderen?
- Welke term wordt gedefinieerd als een lijst van elke nucleotidebasis voor soortenorganismen?
- Septate versus niet-Septate Hyphae
- Wat zijn de belangrijkste intermoleculaire krachten van xenon?
- Hoe een moleculaire motor in een netwerk beweegt
- Brigitte Macron viert eerste panda geboren in Frankrijk
- Welke twee groepen zijn nauw verwant evolutionair planten en dieren schimmels?
- Wie is de beroemdste wetenschapper die de evolutietheorie ontwikkelt?
- Wat is geen belangrijke veronderstelling voor de wetenschappelijke methode?
- Sleutelenzymen voor het synthetiseren van natuurlijke producten
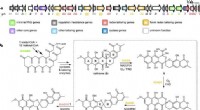
- Onderzoekers ontwikkelen nieuwe strategie voor efficiënte OLED-schermen met actieve matrix

- Grafeen-adsorbaat van der Waals bindingsgeheugen inspireert slimme grafeensensoren
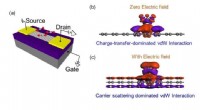
- Het gebruik van reinigingstechnologieën optimaliseren

- Interfaciale chemie verbetert de oplaadbaarheid van Zn-batterijen
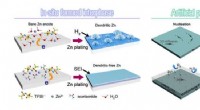
 Waarom worden verbindingen als zuivere stoffen beschouwd?
Waarom worden verbindingen als zuivere stoffen beschouwd?  2017 wordt waarschijnlijk het derde warmste jaar ooit
2017 wordt waarschijnlijk het derde warmste jaar ooit Cellen voeren welk proces uit om te overleven?
Cellen voeren welk proces uit om te overleven?  Wat is de fundamentele theorie van de aardwetenschappen?
Wat is de fundamentele theorie van de aardwetenschappen?  Wat is een bocht in Crustal Rock?
Wat is een bocht in Crustal Rock?  Waar hangt Zygote van voor watervoedingsstoffen?
Waar hangt Zygote van voor watervoedingsstoffen?  'S Werelds eerste video van een ruimte-tijdkristal
'S Werelds eerste video van een ruimte-tijdkristal Is de massa van alle chlooratomen altijd 35,47?
Is de massa van alle chlooratomen altijd 35,47?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

