
Wetenschap
Wat gebeurt er als koper reageert met nitinezuur?
De reactie:
Koper (Cu) reageert met salpeterzuur (HNO₃) om koper (II) nitraat (Cu (NO₃) ₂), stikstofdioxidegas (NO₂) en water (H₂O) te produceren.
De evenwichtige chemische vergelijking is:
Cu + 4Hno₃ → Cu (No₃) ₂ + 2no₂ + 2h₂o
Verklaring:
* salpeterzuur als een oxidatiemiddel: Salpeterzuur werkt als een sterk oxidatiemiddel. Dit betekent dat het gemakkelijk elektronen van andere stoffen accepteert, waardoor ze worden geoxideerd.
* Koperoxidatie: Koper wordt geoxideerd van zijn elementaire toestand (Cu⁰) naar koper (II) ionen (Cu²⁺).
* Stikstofreductie: De stikstof in salpeterzuur wordt gereduceerd van +5 oxidatietoestand in HNO₃ tot +4 oxidatietoestand in NO₂.
* Vorming van kopernitraat: De koper (II) ionen combineren met nitraationen (NO₃⁻) om koper (II) nitraat te vormen, een oplosbare verbinding.
* evolutie van stikstofdioxide: De verminderde stikstofatomen van salpeterzuur vormen stikstofdioxidegas, dat een roodbruin, giftig gas is.
Observaties:
* bruin gas: De reactie produceert een bruin gas, dat stikstofdioxide is (NO₂).
* Blauwe oplossing: Naarmate de reactie vordert, wordt de oplossing blauw vanwege de vorming van koper (II) nitraat.
* Warmteproductie: De reactie is exotherme, wat betekent dat het warmte vrijgeeft.
Waarom geen eenvoudige verplaatsingsreactie?
Je denkt misschien dat koper waterstof uit salpeterzuur zou verplaatsen zoals bij sommige andere zuren. Tikstofzuur is echter een sterk oxidatiemiddel, dus het geeft de voorkeur aan het oxideren van koper in plaats van er door te worden gereduceerd.
Aanvullende opmerkingen:
* De concentratie van het salpeterzuur beïnvloedt de reactie. Geconcentreerd salpeterzuur zal meer stikstofdioxidegas produceren. Verdunde salpeterzuur produceert in plaats daarvan stikstofoxidegas (nee).
* De reactie is vrij krachtig en de geproduceerde dampen moeten met zorg worden behandeld.
Laat het me weten als je meer informatie wilt over een van deze aspecten!
Hoofdlijnen
- De moleculen die extracellulaire signalen omzetten in intracellulaire signalen zijn?
- Wat hebben bacteriën gemeen met cellen en andere levende organismen?
- Gemengde bodembedekkers leggen koolstof vast in de bodem en kunnen de klimaatverandering helpen verminderen
- Op welke manier controleert de samenleving de wetenschap?
- Wat is de extrinsieke route van coagulatie geïnitieerd door?
- Wetenschappelijke tijdschriften tonen weinig handhaving van de rapportagerichtlijnen voor dieronderzoek
- Indringende vraag:Wat doodt de honingbijen?
- Wat is een kenmerk van SAC -schimmels?
- Factoren die de primaire productiviteit beïnvloeden
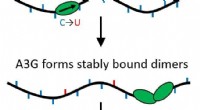
- Een als door te bewerken, twee als door wegversperring:menselijk eiwit bestrijdt HIV als monomeer en dimeer
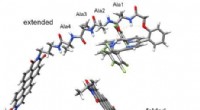
- Picoseconde-elektronenoverdracht in peptiden kan energietechnologieën helpen
- Kristallisatie kristalhelder gemaakt

- Enkele vingerafdruk op plaats delict detecteert klasse A-drugsgebruik

- Metaal-organische raamwerken kunnen ondanks de aanwezigheid van water gassen scheiden

 Minder vooringenomen gezichtsherkenning? Microsoft prijst verbetering, IBM biedt hulp
Minder vooringenomen gezichtsherkenning? Microsoft prijst verbetering, IBM biedt hulp 25 mol zwaveldioxide hoeveel gram zuurstof bevat het?
25 mol zwaveldioxide hoeveel gram zuurstof bevat het?  Hoe kan een niet -lichtgevend lichaam worden gemaakt een voorbeeld geven?
Hoe kan een niet -lichtgevend lichaam worden gemaakt een voorbeeld geven?  Onderzoekers ontdekken dat het toevoegen van zeldzame-aarde-elementen aan piëzo-elektrische kristallen de prestaties drastisch verbetert
Onderzoekers ontdekken dat het toevoegen van zeldzame-aarde-elementen aan piëzo-elektrische kristallen de prestaties drastisch verbetert Hoeveel zonnen zijn er in de ruimte?
Hoeveel zonnen zijn er in de ruimte?  De kosten om aluminium Vs te recyclen. Plastic
De kosten om aluminium Vs te recyclen. Plastic Slavenschipmodel brengt een aangrijpend verhaal tot leven in 3D
Slavenschipmodel brengt een aangrijpend verhaal tot leven in 3D Waar is de beste plek om een zonnepaneel te plaatsen?
Waar is de beste plek om een zonnepaneel te plaatsen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


