
Wetenschap
Wat is het Bohr-Rutherford-diagram voor Silicon Atom?
1. Inzicht in de basis
* protonen en neutronen: De kern van het atoom bevat protonen (positief geladen) en neutronen (geen lading).
* elektronen: Negatief geladen elektronen baan rond de kern in energieniveaus genaamd schelpen.
* Atomisch nummer: Het aantal protonen in een atoom definieert het atoomnummer. Het atoomnummer van Silicon is 14.
* Massienummer: Het massagummer is de som van protonen en neutronen. Het massagummer van Silicon is meestal 28 (hoewel er isotopen zijn).
2. Het tekenen van het diagram
* Nucleus: Teken een grote cirkel in het midden om de kern weer te geven.
* Schrijf in de kern het aantal protonen (14) en neutronen (14, sinds 28 - 14 =14).
* elektronenschalen: Teken concentrische cirkels rond de kern om de elektronenschalen weer te geven.
* shell 1 (k shell): Deze schaal kan maximaal 2 elektronen bevatten. Teken twee elektronen als kleine stippen of cirkels rond de eerste cirkel.
* shell 2 (l shell): Deze schaal kan maximaal 8 elektronen bevatten. Teken acht elektronen rond de tweede cirkel.
* shell 3 (m shell): Deze schaal kan maximaal 18 elektronen bevatten. Teken vier elektronen rond de derde cirkel. (Silicon heeft slechts 4 elektronen in deze schaal).
Dit is hoe uw Bohr-Rutherford-diagram voor silicium eruit zou moeten zien:
`` `
(14p, 14n)
O
/ \
/ \
O ----- o
/ \ / \
O --- o o --- o
/ \ / \
O --- o o --- o
`` `
Sleutelpunten:
* Elk elektron wordt weergegeven door een kleine stip of cirkel.
* De elektronen in elke schaal moeten gelijkmatig op elkaar staan.
* Het is belangrijk om het aantal protonen, neutronen en elektronen in elke schaal nauwkeurig weer te geven.
Belangrijke opmerking: Bohr-Rutherford-diagrammen zijn een vereenvoudigd model van het atoom. Hoewel ze nuttig zijn voor het visualiseren van elektronenopstelling, geven ze niet nauwkeurig het werkelijke complexe gedrag van elektronen weer.
 Nieuw-Zeelanders hebben hun zegje gedaan over klimaatadaptatie:hier zijn ze het eens en oneens
Nieuw-Zeelanders hebben hun zegje gedaan over klimaatadaptatie:hier zijn ze het eens en oneens  Hotdogs:Heeft de klimaatverandering gevolgen voor de populaties Afrikaanse wilde honden?
Hotdogs:Heeft de klimaatverandering gevolgen voor de populaties Afrikaanse wilde honden?  Bodem bevat het geheim om klimaatverandering tegen te gaan
Bodem bevat het geheim om klimaatverandering tegen te gaan Diepe riffen zullen ondiepe koraalriffen waarschijnlijk niet redden
Diepe riffen zullen ondiepe koraalriffen waarschijnlijk niet redden Wat gebeurt er als u bomen blijft kappen?
Wat gebeurt er als u bomen blijft kappen?
Hoofdlijnen
- Wat is een native eiwit?
- Wat is Ceramide?
- Het type levenscyclus dat in planten wordt gezien, wordt genoemd?
- Is het waar of niet waar dat alle cellen dezelfde structuur hebben, maar verschillende functies hebben?
- Waarom krult je haar in de zomer? Een scheikundige legt de wetenschap achter structuur uit
- Welk organisme vormt in een voedselweb het eerste trofische niveau?
- Wat zullen sommige stamcellen worden als ze rijpen tot erytrocyten?
- Wat zijn de twee soorten meristematische weefsels?
- Het team van Rensselaer laat zien hoe je ruwe overheidsdata analyseert
- Omkeerbare plakkerigheid in tandcement is iets om over te lachen
- Duurzamere mortels en beton met optimale thermische en mechanische efficiëntie

- Een nieuwe methode voor de productie van geprotoneerde waterstof

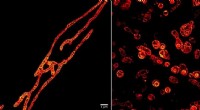
- Levende mitochondriën in ongekend detail gezien:fotobleken in STED-microscopie overwonnen
- Elektronen in het water

 Thuisvoordeel blijft ook in voetbal bestaan zonder fans:studie
Thuisvoordeel blijft ook in voetbal bestaan zonder fans:studie In de VS, kleine biologische melkproducenten kampen met onrust
In de VS, kleine biologische melkproducenten kampen met onrust Hoe sociale media de menselijke beschaving hebben gesynchroniseerd
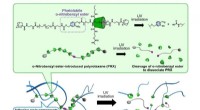
Hoe sociale media de menselijke beschaving hebben gesynchroniseerd  Nieuw synthetisch polymeer afbreekbaar onder zeer milde zure omstandigheden
Nieuw synthetisch polymeer afbreekbaar onder zeer milde zure omstandigheden Zijn de roodverschuivingsgolflengten langer en minder frequent?
Zijn de roodverschuivingsgolflengten langer en minder frequent?  Wat is het volume van het heelal en hoe wordt dit berekend?
Wat is het volume van het heelal en hoe wordt dit berekend?  Alle zonenergie wordt in zijn kern geproduceerd door?
Alle zonenergie wordt in zijn kern geproduceerd door?  Wat is het verschil in wit gat en zwart in astronomie?
Wat is het verschil in wit gat en zwart in astronomie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

